��Ŀ����
����Ŀ��������ѧ֪ʶ���
��1���ڶ�����Ԫ���У���һ�����ܽ���B��O֮���Ԫ���� ��
��2��N��O���������NO2+ �� ���ĵ���ʽΪ �� ��ȵ�������������2�֣���
��3��Ԫ�ؽ�Au���������ڱ��еĵ������ڣ���Cuͬ�壬Auԭ����Χ�����Ų�ʽΪ��
��4��ij�л���ṹ��ͼ��ʾ��������е�ԭ�ӳ�H��������sp3�ӻ���2mol�÷��Ӻ��Цм�����ĿΪ 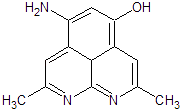
��5����֪Ti3+���γ���λ��Ϊ6���������к��ѵ�������ɫ�ľ��壬һ��Ϊ��ɫ����һ��Ϊ��ɫ�������ʵ��֤�������־������ɽ�ΪTiCl36H2O��Ϊ�ⶨ�����־��廯ѧʽ�����������ʵ�飺
a���ֱ�ȡ����������������ᄃ�����Ʒ��ɴ�����Һ��
b���ֱ���������Һ�е���AgNO3��Һ����������ɫ������
c��������ȫ��ֱ���˵����ݳ�������ϴ�Ӹ���������������ɫ�����ˮ��Һ��AgNO3��Һ��Ӧ�õ��İ�ɫ��������Ϊ��ɫ�����ˮ��Һ��Ӧ�õ�����������1.5��������ɫ���������Ļ�ѧʽΪ �� ����ʾ���ڽ����磩
���𰸡�
��1��Be��C
��2��![]() ��N2O��CO2
��N2O��CO2
��3��5d106s1
��4��5��12NA
��5��[Ti��H2O��5Cl]Cl2?H2O
���������⣺��1��ͬ���ڣ��������ҵ�һ������������ڶ�����Ԫ���У���һ�����ܽ���B��O֮���Ԫ����Be��C�����Դ��ǣ�Be��C��
��2.��N��O���������NO2+ �� ��CO2��Ϊ�ȵ����壬�ṹ���ƣ������ʽΪ ![]() ���ȵ����廹��N2O��SCN����OCN����CNO����CS2��BeCl2�ȣ����Դ��ǣ�
���ȵ����廹��N2O��SCN����OCN����CNO����CS2��BeCl2�ȣ����Դ��ǣ� ![]() ��N2O��CO2��
��N2O��CO2��
��3.����Au���������ڱ��еĵ������ڣ���Cuͬ�壬ΪIB��Ԫ�أ�Auԭ����Χ�����Ų�ʽΪ5d106s1 �� ���Դ��ǣ�5d106s1��
��4.��2������C��������N����OH��O��������״���ĵ�CΪsp3�ӻ�������5��ԭ����sp3�ӻ���˫������1���м�����2mol�÷��Ӻ��Цм�����ĿΪ12NA �� ���Դ��ǣ�5��12NA��
��5.����������е���ԭ���Dz��������ƶ��ģ����������п����γ������ӣ������ӿ����������ӷ�Ӧ�����Ȼ�����ɫ������������ɫ�����ˮ��Һ��AgNO3��Һ��Ӧ�õ��İ�ɫ��������Ϊ��ɫ�����ˮ��Һ��Ӧ�õ�����������1.5����˵����ɫ�����������������ƶ��������ӣ�����ɫ������ֻ��2�������ƶ������ӣ�����һ����ԭ���γ���������Ϊ��Ϊ6��λ������������������ˮ������ѧʽΪ[TiCl��H2O��5]Cl2H2O������ɫ����Ļ�ѧʽΪ[Ti��H2O��6]Cl3 �� ���Դ��ǣ�[Ti��H2O��5 Cl]Cl2H2O��

����Ŀ���±�ΪԪ�����ڱ���һ���֣������г���11��Ԫ�������ڱ��е�λ�ã���Ҫ��������и�С�⣮
���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
2 | �� | �� | �� | |||||
3 | �� | �� | �� | �� | �� | |||
4 | �� | �� |
��1����ѧ��������õ�Ԫ��������Ԫ�ط��ţ�����ԭ�ӽṹʾ��ͼΪ ��
��2��Ԫ�آ������Ϊ��������������ˮ����Ļ�ѧʽΪ ��
��3��Ԫ�آ���Ԫ�آ��γɻ�����ĵ���ʽΪ ��
��4���ǽ�������ǿ��Ԫ��������Ԫ�ط��ţ�����0����ԭ�Ӱ뾶����Ԫ��������Ԫ�ط��ţ���Ԫ�آٵ�����ˮ��Ӧ�����ӷ���ʽ�� ��
��5���١��ۡ�������Ԫ�ص����������ˮ�����У�������ǿ�Ļ�����Ļ�ѧʽ�� ��
��6�����γ��������������Ԫ��������Ԫ�ط��ű�ʾ����д����Ԫ�صĵ�����ٵ�����������ˮ���ﷴӦ�Ļ�ѧ����ʽ