题目内容
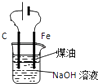
【题目】乙烯催化氧化成乙醛可设计成如图所示的燃料电池,在制备乙醛的同时能获得电能,其总反应为:2CH2═CH2+O2→2CH3CHO.下列有关说法不正确的是( ) 
A.该电池可将化学能转化为电能
B.每有0.1 mol O2反应,则迁移0.4 mol H+
C.正极反应式为:CH2=CH2﹣2e﹣+2OH﹣═CH3CHO+H2O
D.负极区溶液的pH减小
【答案】C
【解析】解:A.原电池工作时,将化学能转化为电能,故A正确;B.由电极方程式O2+4H++4e﹣═2H2O可知,每有0.1molO2反应,则迁移H+0.4mol,故B正确;
C.正极发生还原反应,电极方程式为O2+4H++4e﹣═2H2O,负极为CH2=CH2﹣2e﹣+H2O=CH3CHO+2H+ , 故C错误;
D.负极反应为CH2=CH2﹣2e﹣+H2O=CH3CHO+2H+ , 氢离子浓度增大,溶液的pH减小,故D正确;
故选C.
由总反应式可知CH2=CH2被氧化,应为原电池的负极反应,因电解质溶液呈酸性,则负极电极方程式为CH2=CH2﹣2e﹣+H2O=CH3CHO+2H+ , 正极通入氧气,发生还原反应,电极方程式为O2+4H++4e﹣═2H2O,以此解答该题.

练习册系列答案
相关题目