题目内容
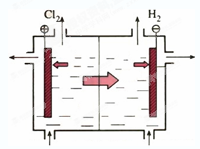
用石墨电极电解500 mL饱和食盐水,通电一定时间后,在一个电极上收集到标准状况下1.12L氯气。
(1)另一电极所得产物的名称是 ,其质量为 ;
(2)转移电子的物质的量为 ;
(3)电解后溶液中OH-的物质的量浓度为 。(假设电解前后溶液体积不变)
(1)另一电极所得产物的名称是 ,其质量为 ;
(2)转移电子的物质的量为 ;
(3)电解后溶液中OH-的物质的量浓度为 。(假设电解前后溶液体积不变)
(1) 氢气(1分);0.1g (2分)(2)0.1mol (2分) (3)0.2 mol·L-1 (2分)
(1)惰性电极电解饱和食盐水,阳极是氯离子失去电子,生成氯气。阴极是氢离子得到电子,生成氢气。根据电子得失守恒可知,生成氢气也是1.12L,物质的量是0.05mol,质量是0.1g。
(2)转移电子是0.05mol×2=0.1mol。
(3)电解的方程式为2NaCl+2H2O 2NaOH+H2+Cl2↑,所以生成氢氧化钠是0.1mol,其浓度是0.1mol÷0.5L=0.2molk/L。
2NaOH+H2+Cl2↑,所以生成氢氧化钠是0.1mol,其浓度是0.1mol÷0.5L=0.2molk/L。
(2)转移电子是0.05mol×2=0.1mol。
(3)电解的方程式为2NaCl+2H2O
 2NaOH+H2+Cl2↑,所以生成氢氧化钠是0.1mol,其浓度是0.1mol÷0.5L=0.2molk/L。
2NaOH+H2+Cl2↑,所以生成氢氧化钠是0.1mol,其浓度是0.1mol÷0.5L=0.2molk/L。
练习册系列答案
相关题目
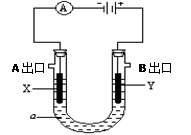
 为直流电源,
为直流电源, 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀槽.接通电路后发现
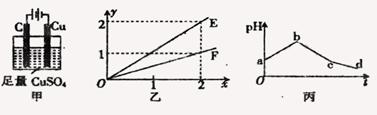
为电镀槽.接通电路后发现 后,使c、d两点短路。下列叙述正确的是( )
后,使c、d两点短路。下列叙述正确的是( )

