题目内容
[化学—选修物质结构和性质](15分)
下表为部分短周期元素的性质或原子结构,已知A—D的原子序数依次增大。
请结合表中信息完成下列各小题(答题时用所对应的元素符号)
A:(1)写出C原子的电子排布图____________
(2)A、B、C、D的第一电离能由大到小的顺序为______________
(3)用电离方程式表示C的最简单氢化物的水溶液呈碱性的原因 _______________
B:按照共价键理论,分子中每个原子的最外电子层电子数均已饱和。已知ABCD分子可能有三种不同结构,它们的结构可以从其他物质的结构中获得启发。
(4)ABC的结构式是___________。向其中插入一个D原子,若形成配位键(用→表示)则ABCD的结构式为______________分子中C的原子的杂化类型是______________;若无配位键则ABCD的结构式为___________分子中D原子的杂化类型为______________。
(5)BD2的电子式是____________将D原子换成等电子的 所得ABCD的结构式为________,分子中C原子的杂化类型是______________。
所得ABCD的结构式为________,分子中C原子的杂化类型是______________。
(6)在ABCD的三种可能结构中B原子的杂化类型__________(填“相同”或“不相同”)
下表为部分短周期元素的性质或原子结构,已知A—D的原子序数依次增大。
| 元素编号 | 元素性质或原子结构 |
| A | A原子所处的周期数、族序数、原子序数均相等 |
| B | 核外电子有6种不同运动状态 |
| C | 最简单氢化物的水溶液呈碱性 |
| D | 基态原子的S轨道电子数等于P轨道电子数 |
A:(1)写出C原子的电子排布图____________
(2)A、B、C、D的第一电离能由大到小的顺序为______________
(3)用电离方程式表示C的最简单氢化物的水溶液呈碱性的原因 _______________
B:按照共价键理论,分子中每个原子的最外电子层电子数均已饱和。已知ABCD分子可能有三种不同结构,它们的结构可以从其他物质的结构中获得启发。
(4)ABC的结构式是___________。向其中插入一个D原子,若形成配位键(用→表示)则ABCD的结构式为______________分子中C的原子的杂化类型是______________;若无配位键则ABCD的结构式为___________分子中D原子的杂化类型为______________。
(5)BD2的电子式是____________将D原子换成等电子的
 所得ABCD的结构式为________,分子中C原子的杂化类型是______________。
所得ABCD的结构式为________,分子中C原子的杂化类型是______________。(6)在ABCD的三种可能结构中B原子的杂化类型__________(填“相同”或“不相同”)
(1)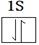
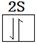
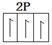 (2分) (2)N>O>C>H (2分)
(2分) (2)N>O>C>H (2分)
(3)NH3·H2O NH4++OH- (2分)
NH4++OH- (2分)


 (4)H—C N H—C N→O SP H—O—C N SP3 (5分)
(4)H—C N H—C N→O SP H—O—C N SP3 (5分)
(5)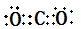 H—N=C=O SP2 (3分) (6)相同(1分)
H—N=C=O SP2 (3分) (6)相同(1分)
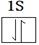
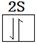
 (2分) (2)N>O>C>H (2分)
(2分) (2)N>O>C>H (2分)(3)NH3·H2O
 NH4++OH- (2分)
NH4++OH- (2分)

 (4)H—C N H—C N→O SP H—O—C N SP3 (5分)
(4)H—C N H—C N→O SP H—O—C N SP3 (5分)(5)
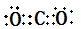 H—N=C=O SP2 (3分) (6)相同(1分)
H—N=C=O SP2 (3分) (6)相同(1分)根据元素的结构及有关性质可知,A是H,B是C,C是N,D是O。
根据构造原理可知,氮原子的基态电子排布图为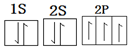
(2)非金属性越强,第一电离能越大,由于氮原子的2p轨道电子处于半充满状态,所以氮原子的第一电离能大于氧原子的,即N>O>C>H。
(3)氨气溶于水生成一水合氨,一水合氨是弱电解质电离出OH-,所以溶液显碱性,方程式为
NH3·H2O NH4++OH- 。
NH4++OH- 。
(4)ABC的化学式为HCN,其结构式为 。由于分子中氮原子还有1对孤对电子,所以能和氧原子形成配位键,即
。由于分子中氮原子还有1对孤对电子,所以能和氧原子形成配位键,即 。如果没有配位键,要满足稳定结构,则氧原子必需分别和氢原子及碳原子形成共价键,即结构式为
。如果没有配位键,要满足稳定结构,则氧原子必需分别和氢原子及碳原子形成共价键,即结构式为 。该化合物分子中氧原子形成的化学键全部是单键,所以氧原子是sp3杂化。
。该化合物分子中氧原子形成的化学键全部是单键,所以氧原子是sp3杂化。
(5)BD2是CO2,分子中含有碳氧双键,电子式为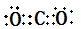 。将D原子换成等电子的
。将D原子换成等电子的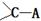 ,则要满足稳定结构,结构式就必需是H—N=C=O,由于该化合物分子氮原子形成1个单键和 1个双键,所以是sp2杂化。
,则要满足稳定结构,结构式就必需是H—N=C=O,由于该化合物分子氮原子形成1个单键和 1个双键,所以是sp2杂化。
(6)在这三种结构中,碳原子都是sp杂化。
根据构造原理可知,氮原子的基态电子排布图为

(2)非金属性越强,第一电离能越大,由于氮原子的2p轨道电子处于半充满状态,所以氮原子的第一电离能大于氧原子的,即N>O>C>H。
(3)氨气溶于水生成一水合氨,一水合氨是弱电解质电离出OH-,所以溶液显碱性,方程式为
NH3·H2O
 NH4++OH- 。
NH4++OH- 。(4)ABC的化学式为HCN,其结构式为
 。由于分子中氮原子还有1对孤对电子,所以能和氧原子形成配位键,即
。由于分子中氮原子还有1对孤对电子,所以能和氧原子形成配位键,即 。如果没有配位键,要满足稳定结构,则氧原子必需分别和氢原子及碳原子形成共价键,即结构式为
。如果没有配位键,要满足稳定结构,则氧原子必需分别和氢原子及碳原子形成共价键,即结构式为 。该化合物分子中氧原子形成的化学键全部是单键,所以氧原子是sp3杂化。
。该化合物分子中氧原子形成的化学键全部是单键,所以氧原子是sp3杂化。(5)BD2是CO2,分子中含有碳氧双键,电子式为
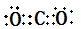 。将D原子换成等电子的
。将D原子换成等电子的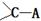 ,则要满足稳定结构,结构式就必需是H—N=C=O,由于该化合物分子氮原子形成1个单键和 1个双键,所以是sp2杂化。
,则要满足稳定结构,结构式就必需是H—N=C=O,由于该化合物分子氮原子形成1个单键和 1个双键,所以是sp2杂化。(6)在这三种结构中,碳原子都是sp杂化。

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
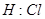
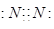
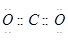
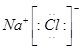
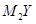 。下列说法正确的是( )
。下列说法正确的是( ) 、M
、M