��Ŀ����
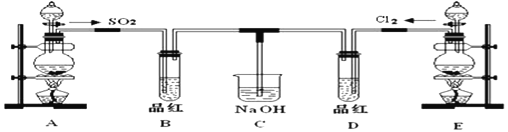
����Ŀ�������Ѿ��ܷⴢ��ʱ��Խ��������Խ�ã�ԭ��֮һ�Ǵ������������������ζ��������ʵ����Ҳ����������ͼ��ʾ��װ����ȡ������������ش��������⡣

(1)�Ҵ������й����ŵ�������_______��
�����еĹ����ŵĽṹ��ʽ ________��
(2)�Թ�a�м��뼸�����Ƭ��Ŀ����____________��
(3)�Թ�a�з�����Ӧ�Ļ�ѧ����ʽΪ_______________________����Ӧ������__________��
(4)��Ӧ��ʼǰ���Թ�b��ʢ�ŵ���Һ��____________��
(5)����____________�ķ������Ƶõ������������������
(6)Ũ��������� _______________________��
���𰸡� �ǻ� ��COOH ��ֹ���� CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O ������ȡ���� ����̼������Һ ��Һ ��������ˮ��
CH3COOCH2CH3+H2O ������ȡ���� ����̼������Һ ��Һ ��������ˮ��
��������(1)���Ĺ��������ǻ����Ҵ��к����ǻ�������Ĺ��������Ȼ����Ȼ��Ľṹ��ʽΪ-COOH���ʴ�Ϊ���ǻ���-COOH��
(2)�Թ�a�м��뼸�����Ƭ���Է�ֹ���У��ʴ�Ϊ����ֹ������
(3)�������Ҵ���Ũ���������¼��ȷ���������Ӧ��������������ˮ��ͬʱ�÷�Ӧ���棬
��Ӧ�Ļ�ѧ����ʽΪCH3COOH+CH3CH2OH![]() CH3COOC2H5+H2O���ʴ�Ϊ��CH3COOH+CH3CH2OH
CH3COOC2H5+H2O���ʴ�Ϊ��CH3COOH+CH3CH2OH![]() CH3COOC2H5+H2O��
CH3COOC2H5+H2O��
(4)�Ʊ���������ʱ���ñ���̼������Һ����������������ȥ�Ҵ������ᡢ���������������ܽ�ȣ����ڷֲ㣬�ʴ�Ϊ������̼������Һ��
(5)�������������ڱ���̼������Һ�����÷�Һ�������룬�ʴ�Ϊ����Һ��
(6)��ʵ����Ũ���������Ϊ��������ˮ�����ʴ�Ϊ����������ˮ����