题目内容
【题目】Ⅰ.对于混合物的分离或提纯,常采用的方法有:①过滤、②蒸发、③蒸馏、④萃取、⑤加热分解等。下列各组混和物的分离或提纯应采用什么方法?(填序号)
(1)提取碘水中的碘 ___________(2)除去食盐溶液中的水 ___________
(3)淡化海水 ___ ______ (4)KCl中含有KClO3 。
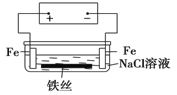
Ⅱ.根据以下装置图,回答下列问题:

写出仪器名称 ② ③ ;仪器①~④中,使用时必须检查是否漏水的有 (填序号)。
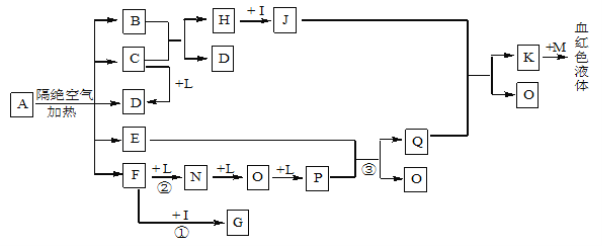
Ⅲ.某课外活动小组设计下列实验装置,验证“二氧化碳与水接触时才能和过氧化钠反应”。
(1)过氧化钠与水反应的化学方程式是 。
(2)装置Ⅰ是制备纯净的 ,则仪器①和②中最适宜的试剂组合是________(填字母)
a.稀盐酸 b.稀硫酸 c.小苏打 d.石灰石
(3)实验时,应先打开弹簧夹K2,关闭K1,观察到预期现象后,打开K1 ,再关闭K2。
(4)实验过程中将带火星的木条置于a口,观察到带火星的木条始终不复燃。
①为观察到最终木条复燃,甲建议在Ⅲ后安装一个盛有碱石灰的干燥管,目的是 ;
②乙认为即使采纳甲的建议且最终观察到木条复燃,也不能证明CO2参与了反应,原因是 。
(5)为进一步达到实验目的,应补充的实验是:取最终反应后Ⅲ中所得固体, 。
【答案】Ⅰ.(1)④ (2)② (3)③ (4) ⑤
Ⅱ.冷凝管 分液漏斗 ③④
Ⅲ.(1)2Na2O2 +2H2O=4NaOH+O2 ↑
(2) CO2 bc
(4)①除去未充分反应的CO2 ②水与Na2O2反应生成氧气
(5)加入稀盐酸,将产生的气体通入澄清石灰水中(答案合理即可)
【解析】
试题分析:Ⅰ.(1)从碘水中得到碘,利用碘易溶于有机溶剂,常采用萃取的方法,即选项④正确;(2)常采用蒸发方法得到食盐,故选项②正确;(3)淡化海水常采用蒸馏方法,故选项③正确;(4)利用KClO3的受热分解,故选项⑤正确。
Ⅱ.由图可知,②为冷凝管,③为分液漏斗,故答案为:冷凝管;分液漏斗;仪器①~④中,使用时必须检查是否漏水的有分液漏斗和容量瓶,故答案为:③④;
Ⅲ.(1)过氧化钠与水反应生成氢氧化钠和氧气,方程式为:2Na2O2 +2H2O=4NaOH+O2 ↑;
(2)装置Ⅰ是制备纯净的CO2,因盐酸和碳酸钙反应时可能会带出一部分氯化氢,为了使实验更准确应该可用稀硫酸和小苏打反应制二氧化碳,故答案为:bc;
(4)①二氧化碳不支持燃烧,也不能燃烧,当二氧化碳通过过氧化钠时,不可能全部反应,所以应该除去二氧化碳,再用带火星的木条来检验是否产生了氧气,否则氧气浓度高低而导致带火星的木条不复燃,故答案为:除去未充分反应的CO2;②生成的二氧化碳中含有水蒸气,水也能够和过氧化钠反应生成氧气,干扰二氧化碳和过氧化钠的反应,故答案为:水与Na2O2反应生成氧气;
(5)Ⅲ中固体若有碳酸钠,盐酸可以和碳酸钠反应生成二氧化碳,二氧化碳能使澄清石灰水变混浊,故答案为:加入稀盐酸,将产生的气体通入澄清石灰水

【题目】选修3——物质结构与性质
已知X、Y、Z、R、Q为周期表中原子序数依次增大的前36号元素,相关信息如下:
X元素是宇宙中最丰富的元素 |
Y元素基态原子的核外p电子数比s电子数少1 |
Z元素被誉为“太空金属”,也有“生物金属”之称,其基态原子次外层有2个未成对电子 |
R元素在元素周期表的第十一列 |
Q元素在周期表里与R元素在同一个分区 |
请回答下列问题:
(1)YX3中心原子的杂化轨道类型是 ,离子化合物YX5的电子式是 。
(2)CO与Y2属于等电子体,1 个CO分子中含有的π键数目是 个。
(3)工业上利用ZO2和碳酸钡在熔融状态下制取化合物A(A可看做一种含氧酸盐),A晶体的晶胞为正方体(如图1)。
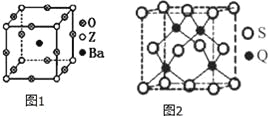
①制备A的化学反应方程式是 ;
②在A晶体中,Z的配位数为 ;
(4)R2+离子的外围电子层电子排布式为 。R2O的熔点比R2S的 (填“高”或“低”)。
(5)Q元素和硫(S)元素能够形成化合物B,B晶体的晶胞为正方体(如图2),若晶胞棱长为5.4×10-8cm,则晶胞密度为 gcm﹣3(列式并计算)。