��Ŀ����
����Ŀ�������������ʹ�õĽ���֮һ��������ѧ֪ʶ���ش��������⡣
��1����FeCl3��Һ�����ˮ�����Ƶ�Fe(OH)3���塣����Fe(OH)3�����FeCl3��Һ�ķ�����____________________________________��
��2������������������ɢϵ�ı���������__________________________________��
��3�����岻�����������������Գ���������������ȱ����ƶѪ�����Ͳ�����ͬʱ����ά����C��ԭ��__________________________________________________��
��4�����ӹ�ҵ��FeCl3��Һ��ʴ���ھ�Ե���ϵ�ͭ������ӡˢ��·�壬��д��FeCl3��Һ��ͭ��Ӧ�����ӷ���ʽ__________________________________________��
����ʦ��������ӡˢ��·��ķ�ˮ�л���ͭ�������FeCl3��Һ��������·�����
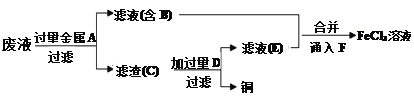
����������Ʒ����������ѧ֪ʶ�ش��������⡣
��5��������ҺE�н��������ӵķ�����___________________________________��
��6��ͨ��F������Ӧ�����ӷ���ʽΪ_____________________________________��
���𰸡� ��ƽ�й��������ַ�ɢϵ�������ö����ЧӦ�� ��ɢ������ֱ����1nm-100nm֮�� ����ά����C���Ա����������������������������ٽ�ҩ������գ�����ά����C�л�ԭ�ԣ���ֹ�����������ȣ� 2Fe3++Cu��2Fe2++Cu2+ �μ�KSCN�ޱ仯���ٵμ���ˮ����˫��ˮ����Ѫ��ɫ����Fe2+����μ�K3[Fe(CN)6]��������ɫ��������Fe2+��μ�NaOH��Һ���������������ɰ�ɫѸ�ٱ�Ϊ����ɫ������Ϊ���ɫ,����Fe2+�� 2Fe2++Cl2��2Fe3++2Cl��
����������1������Fe(OH)3�����FeCl3��Һ�ķ��������ö����ЧӦ��������Բ��������ЧӦ����2������������������ɢϵ�ı��������Ƿ�ɢ������ֱ����1nm��100nm֮�䡣��3��ά����C���л�ԭ�ԣ�����ά����C���Ա����������������������������ٽ�ҩ������ա���4��FeCl3��Һ��ͭ��Ӧ�����ӷ���ʽΪ2Fe3++Cu��2Fe2++Cu2+����5����Һ�к��������ӡ�ͭ���ӡ��������ӣ�����������û���ͭ������C��Ϊͭ�������������������ܽ������˵õ�ͭ����ҺE�ϲ���ͨ�����������Ȼ�����������ҺE���������ӵķ���������K3[Fe(CN)6]����ȡ������Һ���Թ��У��μ�K3[Fe(CN)6]������ɫ��������6��ͨ������������Ӧ�����ӷ���ʽΪ2Fe2++Cl2��2Fe3++2Cl����

 Ʒѧ˫�ž�ϵ�д�
Ʒѧ˫�ž�ϵ�д� Сѧ��ĩ���100��ϵ�д�
Сѧ��ĩ���100��ϵ�д� ��ĩ��ϰ���ϵ�д�
��ĩ��ϰ���ϵ�д� ����ѧ�䵥Ԫ������ĩר����100��ϵ�д�
����ѧ�䵥Ԫ������ĩר����100��ϵ�д�