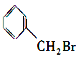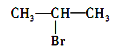题目内容
【题目】有机玻璃(PMMA)是一种具有优良的光学性、耐腐蚀性的高分子聚合物,其合成路线之一如图所示:

请回答下列问题:
(1)写出检验A中官能团所需试剂及现象__、__。
(2)用系统命名法给B命名__。
(3)写出C与足量的NaOH乙醇溶液,在加热条件下反应的化学方程式__。
(4)写出E生成PMMA反应的化学方程式__。
(5)下列说法正确的是__。
a.B的核磁共振氢谱有3组峰,峰面积比为6∶1∶1
b.B→C的反应类型为取代反应
c.D中存在顺反异构
d.1molPMMA发生水解反应时消耗1molNaOH
【答案】银氨溶液[或Ag(NH3)2OH] 加热后有银镜产生[或新制Cu(OH)2悬浊液,加热后有红色沉淀产生] 2-甲基丙酸  +2NaOH
+2NaOH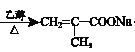 +NaCl+2H2O n
+NaCl+2H2O n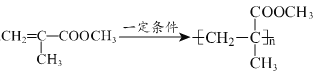 ab
ab
【解析】
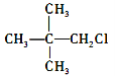
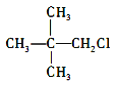
根据C的结构简式,可判断B中含有羧基,则B的结构简式为![]() ;C在NaOH/醇加热的条件下发生消去反应,则D的结构简式为
;C在NaOH/醇加热的条件下发生消去反应,则D的结构简式为![]() ;D与甲醇发生酯化反应,生成
;D与甲醇发生酯化反应,生成![]() ;再发生加聚反应即可生成PMMA。
;再发生加聚反应即可生成PMMA。
(1)A中含有的官能团为醛基,可用银氨溶液[或Ag(NH3)2OH],现象为加热后有银镜产生(或新制Cu(OH)2悬浊液,加热后有红色沉淀产生);
(2)分析可知,B的结构简式为![]() ,系统命名法的名称为2-甲基丙酸;
,系统命名法的名称为2-甲基丙酸;
(3) C与足量的NaOH乙醇溶液在加热的条件下发生消去反应及羧酸的中和反应,方程式为![]() +2NaOH
+2NaOH![]()
![]() +NaCl+2H2O;
+NaCl+2H2O;
(4)E的结构简式为![]() ,在一定条件下发生加聚反应生成PMMA,方程式为n
,在一定条件下发生加聚反应生成PMMA,方程式为n ;
;
(5) a.B的结构简式为![]() ,核磁共振氢谱有3组峰,峰面积比为6∶1∶1,a正确;
,核磁共振氢谱有3组峰,峰面积比为6∶1∶1,a正确;
b.B→C为Cl原子取代H的反应,反应类型为取代反应,b正确;
c.D的结构简式为![]() ,只连接2个不同的原子团,不存在顺反异构,c错误;
,只连接2个不同的原子团,不存在顺反异构,c错误;
d.1molPMMA发生水解反应时消耗nmolNaOH,d错误;
答案为ab。

【题目】“绿水青山就是金山银山”。目前人们对环境保护、新能源开发很重视,研究NO2、NO、CO、SO2等大气污染物转化为能参与大气循环的物质,对建设美丽中国具有重要意义。
(1)有人设计通过硫循环完成CO的综合处理,原理为
a.2CO(g)+SO2(g)![]() S(l)+2CO2(g) △H1= - 37.4kJ·mol-1
S(l)+2CO2(g) △H1= - 37.4kJ·mol-1
b.S(l)+2H2O(g)![]() 2H2(g)+SO2(g) △H2=-45.4 kJ·mol-1
2H2(g)+SO2(g) △H2=-45.4 kJ·mol-1
则CO和水蒸气完全反应生成H2和CO2的热化学方程式为__________________________________。
(2)CO可在一定条件下转化为CH3OH。已知:向2L密闭容器中通入2 molCO和4molH2,在适合的催化剂和T1温度下,发生反应CO(g)+2H2(g)![]() CH3OH(g) △H<0,10min时达到平衡状态,10min后改变温度为T2,20min时达到平衡状态,反应过程中部分数据见表:
CH3OH(g) △H<0,10min时达到平衡状态,10min后改变温度为T2,20min时达到平衡状态,反应过程中部分数据见表:
反应时间 | CO(mol) | H2(mol) | CH3OH(mol) |
0min | 2 | 4 | 0 |
10min | 2 | ||
20min | 0.2 |
①前10min内的平均反应速率v(CO)= _______;在20min时,温度T2下,该反应的化学平衡常数为________________。
②若30min时升高温度,化学平衡常数值_______(填:“增大“减小”“不变”)。
③在T1温度下,既能增大反应速率和提高CO平衡转化率的措施有_____________(填两种措施即可)
④在恒温恒容下,下列可以判断CO(g)+2H2(g)![]() CH3OH(g)反应达到平衡状态的________(填序号)。
CH3OH(g)反应达到平衡状态的________(填序号)。
a.2v正(H2)=v逆(CH3OH) b.混合气体的物质的量不再变化
c.单位时间内有1 mol CO消耗同时消耗2molH2 d.混合气体的平均相对分子质量不变
(3)已知反应2NO(g)+O2(g)![]() 2NO2的正反应速率v正=k1Cm(NO)Cn(O2),其中k1为速率常数,可通过下表实验数据计算k1、m、n。
2NO2的正反应速率v正=k1Cm(NO)Cn(O2),其中k1为速率常数,可通过下表实验数据计算k1、m、n。
组别 | 起始浓度/mol·L-1 | 初始速率/ mol·L-1·S-1 | |
NO | O2 | ||
1 | 0.02 | 0.0125 | 7.98×10-3 |
2 | 0.02 | 0.0250 | 15.96×10-3 |
3 | 0.04 | 0.0125 | 31.92×10-3 |
则k1=____, m =_____, n =_____。
【题目】四种短周期元素X、Y、Z和W在周期表中的位置如图所示,原子序数之和为48。下列说法不正确的是( )
X | Y | |
Z | W |
A.原子半径大小比较:r(X)>r(Y)
B.X和W可形成共价化合物XW3
C.W的非金属性比Z的弱
D.Z的最低价单核阴离子的失电子能力比Y的强