题目内容
(2013?临沭县模拟)氨既是实验室中常用试剂,也是工业上重要原料.
(1)某学习小组欲制备少量的氨水.供选用的试剂有:①NH4Cl ②(NH4)2CO3.提供的装置如下:
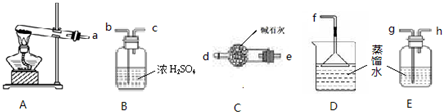
请回答下列问题:
①装置A试管内发生反应的化学方程式为
②从提供的仪器中选择并组装一套本实验的合理、简洁装置,按气流方向连接顺序为(用图中标注的导管口符号表示)a→
(2)氨在氧气中燃烧,生成水和一种单质.
已知:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1
2H2(g)+O2(g)=2H2O(l)△H=-572kJ?mol-1
试写出氨在氧气中燃烧生成液态水和气态单质的热化学方程式
(3)在一定条件下,将1molN2和3molH2混合于一个10L的密闭容器中发生反应N2+3H2
2NH3,5min后达到平衡,平衡时氨的体积分数为25%.
①该反应的平衡常数表达式
②从反应开始到平衡时,N2的反应速率v(N2)=
③H2的转化率为
(4)为检验氨气与酸反应得到的某种常见氮肥的成分,某同学进行了以下实验:①加热氮肥样品产生气体,其中一种气体能使湿润的红色石蕊试纸变蓝,另一种气体能使澄清石灰水变浑浊.②取少量该氮肥样品溶于水,并加入少量BaCl2溶液,没有明显变化.由此可知该氮肥的主要成分可能是
A.NH4Cl B.(NH4)2CO3 C.NH4HCO3 D.NH4NO3.
(1)某学习小组欲制备少量的氨水.供选用的试剂有:①NH4Cl ②(NH4)2CO3.提供的装置如下:

请回答下列问题:
①装置A试管内发生反应的化学方程式为
(NH4)2CO3
2NH3↑+CO2↑+H2O
| ||
(NH4)2CO3
2NH3↑+CO2↑+H2O
| ||
②从提供的仪器中选择并组装一套本实验的合理、简洁装置,按气流方向连接顺序为(用图中标注的导管口符号表示)a→
edf
edf
.(2)氨在氧气中燃烧,生成水和一种单质.
已知:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1
2H2(g)+O2(g)=2H2O(l)△H=-572kJ?mol-1
试写出氨在氧气中燃烧生成液态水和气态单质的热化学方程式
4NH3(g)+3O2(g)=2N2(g)+6H2O(l)△H=-1531.2kJ?mol-1
4NH3(g)+3O2(g)=2N2(g)+6H2O(l)△H=-1531.2kJ?mol-1
.(3)在一定条件下,将1molN2和3molH2混合于一个10L的密闭容器中发生反应N2+3H2
| 催化剂 |
| 高温高压 |
①该反应的平衡常数表达式
K=
| c2(NH3) |
| c(N2)?c3(H2) |
K=
.| c2(NH3) |
| c(N2)?c3(H2) |
②从反应开始到平衡时,N2的反应速率v(N2)=
0.008mol/(L﹒min)
0.008mol/(L﹒min)
.③H2的转化率为
40%
40%
.(4)为检验氨气与酸反应得到的某种常见氮肥的成分,某同学进行了以下实验:①加热氮肥样品产生气体,其中一种气体能使湿润的红色石蕊试纸变蓝,另一种气体能使澄清石灰水变浑浊.②取少量该氮肥样品溶于水,并加入少量BaCl2溶液,没有明显变化.由此可知该氮肥的主要成分可能是
C
C
.A.NH4Cl B.(NH4)2CO3 C.NH4HCO3 D.NH4NO3.
分析:(1)①根据碳酸铵加热分解产生氨气、水和二氧化碳;
②根据题干可知将氨气溶于水形成氨水,生成的氨气需通过碱石灰除去二氧化碳、再通入水中即可;
(2)根据盖斯定律来解答;
(3)①化学平衡常数是平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值;
②设参加反应的氮气的物质的量,再根据三段法求出各自的物质的量,再根据体积分数求出未知数,然后根据v=
计算反应速率;
③根据转化率的概念进行计算;
(4)①加热氮肥样品生成两种气体,其中一种气体能使湿润的红色石蕊试纸变蓝,该气体为氨气,说明含有铵根离子,另一种气体能使澄清石灰水变浑浊,说明碳酸根离子或碳酸氢根离子,②取少量该氮肥样品溶于水,并加入少量BaCl2溶液,没有明显变化,说明没有碳酸氢根离子,由此推导出氮肥的主要成分.
②根据题干可知将氨气溶于水形成氨水,生成的氨气需通过碱石灰除去二氧化碳、再通入水中即可;
(2)根据盖斯定律来解答;
(3)①化学平衡常数是平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值;
②设参加反应的氮气的物质的量,再根据三段法求出各自的物质的量,再根据体积分数求出未知数,然后根据v=
| △c |
| △t |
③根据转化率的概念进行计算;
(4)①加热氮肥样品生成两种气体,其中一种气体能使湿润的红色石蕊试纸变蓝,该气体为氨气,说明含有铵根离子,另一种气体能使澄清石灰水变浑浊,说明碳酸根离子或碳酸氢根离子,②取少量该氮肥样品溶于水,并加入少量BaCl2溶液,没有明显变化,说明没有碳酸氢根离子,由此推导出氮肥的主要成分.
解答:解:(1)①碳酸铵加热分解产生氨气、水和二氧化碳,化学方程式为:(NH4)2CO3
2NH3↑+CO2↑+H2O,故答案为:(NH4)2CO3
2NH3↑+CO2↑+H2O;
②将氨气溶于水形成氨水,生成的氨气需通过碱石灰除去二氧化碳、再通入水中即可,故答案为:edf;
(2)①N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1
②2H2(g)+O2(g)=2H2O(l)△H=-572kJ?mol-1
根据盖斯定律,由②×3-①×2得:4NH3(g)+3O2(g)=2N2(g)+6H2O(l)△H=-1531.2 kJ?mol-1
故答案为:4NH3(g)+3O2(g)=2N2(g)+6H2O(l)△H=-1531.2 kJ?mol-1;
(3)①该反应的平衡常数表达式K=
,故答案为:
;
②设参加反应的氮气的物质的量xmol,
N2 +3H2
2NH3
开始(mol):1 3 0
变化(mol):x 3x 2x
平衡(mol):1-x 3-3x 2x
5min后达到平衡,平衡时氨的体积分数为
×100%=25%,解:x=0.4,
N2的反应速率v(N2)=
=0.008mol/(L﹒min),故答案为:0.008mol/(L﹒min);
③H2的转化率为
×100%=40%,故答案为:40%;
(4)①加热氮肥样品生成两种气体,其中一种气体能使湿润的红色石蕊试纸变蓝,该气体为氨气,说明含有铵根离子,另一种气体能使澄清石灰水变浑浊,说明碳酸根离子或碳酸氢根离子;②取少量该氮肥样品溶于水,并加入少量BaCl2溶液,没有明显变化,说明没有碳酸氢根离子,说明盐中含有铵根离子和碳酸根离子,所以氮肥的主要成分NH4HCO3,故选:C.
| ||
| ||
②将氨气溶于水形成氨水,生成的氨气需通过碱石灰除去二氧化碳、再通入水中即可,故答案为:edf;
(2)①N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1
②2H2(g)+O2(g)=2H2O(l)△H=-572kJ?mol-1
根据盖斯定律,由②×3-①×2得:4NH3(g)+3O2(g)=2N2(g)+6H2O(l)△H=-1531.2 kJ?mol-1
故答案为:4NH3(g)+3O2(g)=2N2(g)+6H2O(l)△H=-1531.2 kJ?mol-1;
(3)①该反应的平衡常数表达式K=
| c2(NH3) |
| c(N2)?c3(H2) |
| c2(NH3) |
| c(N2)?c3(H2) |
②设参加反应的氮气的物质的量xmol,
N2 +3H2
| 催化剂 |
| 高温高压 |
开始(mol):1 3 0
变化(mol):x 3x 2x
平衡(mol):1-x 3-3x 2x
5min后达到平衡,平衡时氨的体积分数为
| 2x |
| 1-x+3-3x+2x |
N2的反应速率v(N2)=
| ||
| 5min |
③H2的转化率为
| 1.2mol |
| 3mol |
(4)①加热氮肥样品生成两种气体,其中一种气体能使湿润的红色石蕊试纸变蓝,该气体为氨气,说明含有铵根离子,另一种气体能使澄清石灰水变浑浊,说明碳酸根离子或碳酸氢根离子;②取少量该氮肥样品溶于水,并加入少量BaCl2溶液,没有明显变化,说明没有碳酸氢根离子,说明盐中含有铵根离子和碳酸根离子,所以氮肥的主要成分NH4HCO3,故选:C.
点评:本题是道综合题,难度不大,涉及知识点较多,注意对应知识的积累.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
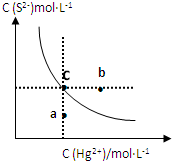 (2013?临沭县模拟)硫化汞(HgS)难溶于水,在自然界中呈红褐色,常用于油画颜料、印泥等.某温度时,HgS在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
(2013?临沭县模拟)硫化汞(HgS)难溶于水,在自然界中呈红褐色,常用于油画颜料、印泥等.某温度时,HgS在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
 (R、R′可以是烃基或H原子)
(R、R′可以是烃基或H原子)

