题目内容
【题目】NA为阿伏加德罗常数的值。下列说法正确的是( )
A. 100mL12mol/L的浓硝酸与过量Cu反应转移电子数目为0.6NA
B. 将1molCl2通入水中,HClO、Cl-、ClO-粒子数之和为2NA
C. 同温同压下,两个等体积的干燥圆底烧瓶中分别充满①HCl ②NO2 ,进行喷泉实验。经充分反应后烧瓶内溶质的物质的量浓度之比为3:2
D. 实验室里要用480 mL 0.1mol/L的硫酸铜溶液,需称取12.5克胆矾配制成溶液
【答案】D
【解析】100mL12mol/L的浓硝酸与过量Cu反应,还原产物为NO2、NO的混合物,转移电子数目大于0.6NA,故A错误;氯水中含有氯分子,将1molCl2通入水中, HClO、Cl-、ClO-粒子数之和小于2NA,故B错误;设容器体积是vL,则气体的物质的量是![]() ;①HCl进行喷泉实验得到溶液的体积是VL,盐酸的浓度是
;①HCl进行喷泉实验得到溶液的体积是VL,盐酸的浓度是![]() ;②NO2进行喷泉实验后发生反应
;②NO2进行喷泉实验后发生反应![]() , 得到硝酸溶液的体积是
, 得到硝酸溶液的体积是![]() ,生成硝酸的物质的量为
,生成硝酸的物质的量为![]() ,硝酸的浓度是
,硝酸的浓度是![]() ,溶质的物质的量浓度之比为1:1,故C错误;实验室里要用480 mL 0.1mol/L的硫酸铜溶液,需用500 mL容量瓶,需胆矾0.5L×0.1mol/L×250g/mol=12.5克,故D正确。
,溶质的物质的量浓度之比为1:1,故C错误;实验室里要用480 mL 0.1mol/L的硫酸铜溶液,需用500 mL容量瓶,需胆矾0.5L×0.1mol/L×250g/mol=12.5克,故D正确。

【题目】【2017·浙江杭州区模拟】 将绿矾(FeSO47H2O)隔绝空气条件下加强热分解,已知产物全部为氧化物,为探究绿矾分解的反应产物,某同学进行了以下实验:
【实验一】为探究固体产物中铁元素的价态,该同学将固体产物溶于足量的稀硫酸得到相应的溶液,进行以下猜想和实验:
猜想 | 实验操作 | 预期现象 |
猜想一:铁元素只显 价 | ① 取溶液样品,滴入KSCN溶液; ②取溶液样品,滴入稀酸性KMnO4溶液 | 加入KSCN溶液无明显现象 稀酸性KMnO4溶液颜色 |
猜想二:铁元素只显 价 | 加入KSCN溶液呈 色; 稀酸性KMnO4溶液颜色无变化 | |
猜想三:铁元素显+2,+3价 | 加入KSCN溶液呈血红色; 稀酸性KMnO4溶液颜色褪色 |
【实验二】为进一步探究该反应的产物,进行了如下图所示的实验
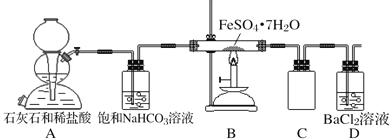
(1)实验开始时,点燃C处酒精喷灯之前应先打开A处活塞通CO2,其目的是 。
(2)饱和NaHCO3的作用是 ;
(3)该组同学称取了55.6克绿矾按如图装置进行试验,待绿矾分解完全后,测得D瓶中沉淀的质量为23.3克,根据这些数据,可以得知,绿矾分解的化学方程式为为 。
(4)该组同学设计的装置存在着一个明显的缺陷是 。