题目内容
向BaCl2溶液中通入SO2至饱和,此过程无明显实验现象。下列说法正确的是( )
| A.向溶液中加入FeCl3溶液,产生的沉淀是亚硫酸钡 |
| B.向溶液中加入稀氨水,产生的沉淀是硫酸钡 |
| C.向溶液中加入AgNO3溶液,产生的沉淀是氯化银 |
| D.向溶液中加入NH4Cl溶液,产生亚硫酸钡沉淀 |
C
解析试题分析:氯化铁具有氧化性,能把SO2氧化生成硫酸,进而生成硫酸钡白色沉淀,A不正确;氨水能和SO2反应生成亚硫酸铵,进而生成亚硫酸钡白色沉淀,B不正确;硝酸银能和氯化钡反应生成白色沉淀氯化银,C正确;向溶液中加入NH4Cl溶液,不会产生沉淀,D不正确,答案选C。
考点:考查SO2的性质以及有关沉淀生成的判断
点评:该题是中等难度的试题,试题综合性强,贴近高考,旨在培养学生分析、归纳和总结问题的能力,有利于培养学生的逻辑思维能力和发散思维能力。

练习册系列答案
相关题目
学生甲和学生乙完成了下列实验,其中实验现象完全相同的是( )
|
| A、选项A | B、选项B |
| C、选项C | D、选项D |
下列实验现象及相关的离子方程式均正确的是( )
| A、碳酸钙粉末中加入醋酸溶液,固体逐渐减少,生成无色气体:CaCO3+2H+?Ca2++CO2↑+H2O | ||
| B、向BaCl2溶液中通入SO2气体,出现白色沉淀:Ba2++SO2+H2O?BaSO3↓+2H+ | ||
C、向H2O2溶液中滴加酸化的KMnO4溶液,KMnO4溶液褪色:2MnO
| ||
D、将等物质的量浓度、等体积的Ba(OH)2溶液和NaHSO4溶液混合,生成白色沉淀:Ba2++SO
|
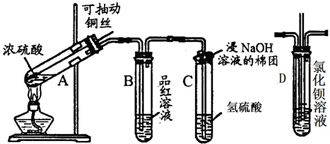
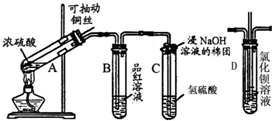 下列是与硫元素相关的一系列实验,根据图所示实验回答下列问题:
下列是与硫元素相关的一系列实验,根据图所示实验回答下列问题: