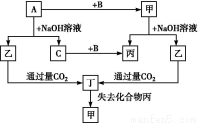
题目内容
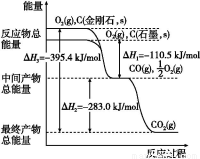
(1)如图表示金刚石、石墨在相关反应过程中的能量变化关系。
写出石墨转化为金刚石的热化学方程式 。
(2)已知:Ti(s)+2Cl2(g) TiCl4(l)ΔH=-804.2 kJ/mol
TiCl4(l)ΔH=-804.2 kJ/mol
2Na(s)+Cl2(g)=2NaCl(s) ΔH=-882.0 kJ/mol
Na(s)=Na(l) ΔH=+2.6 kJ/mol
则TiCl4(l)+4Na(l)=Ti(s)+4NaCl(s)的ΔH= kJ/mol。
(3)已知:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)ΔH=-a kJ/mol
②CH3OH(l)+O2(g)=CO(g)+2H2O(l)ΔH=-b kJ/mol
③H2O(g)=H2O(l) ΔH=-c kJ/mol则:2CO(g)+O2(g) 2CO2(g)的ΔH= kJ/mol。
2CO2(g)的ΔH= kJ/mol。
(4)工业上在催化剂作用下可利用CO合成甲醇:CO(g)+2H2(g)=CH3OH(g),下图表示反应过程中能量的变化情况。
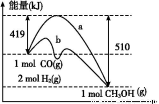
在图中,曲线 (填“a”或“b”)表示使用了催化剂;该反应属于 (填“吸热”或“放热”)反应。
(1)C(石墨,s) C(金刚石,s) ΔH=+1.9 kJ/mol
C(金刚石,s) ΔH=+1.9 kJ/mol
(2)-970.2 (3)(-a+2b-4c) (4)b 放热
【解析】(1)由图像可写出①C(金刚石,s)+O2(g)=CO2(g)ΔH=-395.4 kJ/mol。②C(石墨,s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol,由②-①得C(石墨,s)=C(金刚石,s),其ΔH=-393.5 kJ/mol-(-395.4 kJ/mol)=+1.9 kJ/mol。
(2)根据盖斯定律可将(第二个热化学方程式×2)减去(第一个热化学方程式)再减去(第三个热化学方程式×4)得,ΔH=-882.0 kJ/mol×2-(-804.2 kJ/mol)-(+2.6 kJ/mol)×4=-970.2 kJ/mol。
(3)将①-②×2+③×4得:2CO(g)+O2(g)=2CO2(g) ΔH=-a kJ/mol-(-b kJ/mol×2)+(-c kJ/mol×4)=(-a+2b-4c)kJ/mol。
(4)根据图示可知反应物的总能量大于生成物的总能量,故该反应是放热反应,加入催化剂改变反应历程,降低反应所需的活化能,故b曲线表示使用了催化剂。

 教材全解字词句篇系列答案
教材全解字词句篇系列答案下表是三种难溶金属硫化物的溶度积常数(25 ℃)。
化学式 | FeS | CuS | MnS |
溶度积 | 6.3×10-18 | 1.3×10-36 | 2.5×10-13 |
下列有关说法中正确的是( )
A.25 ℃时,CuS的溶解度大于MnS的溶解度
B.25 ℃时,饱和CuS溶液中,Cu2+的浓度为1.3×10-36 mol/L
C.因为H2SO4是强酸,所以反应CuSO4+H2S CuS↓+H2SO4不能发生
CuS↓+H2SO4不能发生
D.除去某溶液中的Cu2+,可以选用FeS作沉淀剂