��Ŀ����
17�����ᣨH2C2O4�����������һ�ִ�л�����������κͼ���������ˮ���������������ˮ����֪���ᾧ�壨H2C2O4•2H2O��Ϊ��ɫ���壬������ˮ���۵�Ϊ101�棬������ˮ��������170�����Ϸֽ⣮�Իش��������⣺��1������ͬѧ������ͼ1��ʾ��װ�ã�ͨ��ʵ�������ᾧ��ķֽ���װ��A�д��Թܹܿ�������бû���������û��������װ��C�п��Թ۲쵽������Ϊ���ܿ�������ð��������ʯ��ˮ����ǣ��ɴ˿�֪���ᾧ��ֽ�IJ�������CO2��
��2������ͬѧ��Ϊ���ᾧ��ֽ�IJ����к���CO��Ϊ������֤��ѡ�ü���ʵ���е�װ��A��B����ͼ2��ʾ�IJ���װ�ã������ظ�ѡ�ã�����ʵ�飮
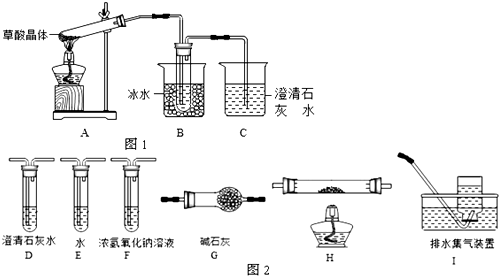
������ͬѧ��ʵ��װ���У��������ӵĺ���˳��Ϊ��
A��B��F��D��G��H��D��I
װ��H��Ӧ����ʢ�е����ʵ�����������ͭ��
����֤�����ᾧ��ֽ��������CO�������ǣ�H֮ǰ��Dװ���г���ʯ��ˮ������ǣ�H�к�ɫ��ĩ��Ϊ��ɫ��H֮���Dװ���г���ʯ��ˮ����ǣ�
���� ��1�����������ʱ���ǵ�������ܺ��нᾧˮ���Լ���ֹ��Ӧ��ˮ���ɣ��Թܿ�Ӧ������б��ʵ���й۲쵽װ��C�б���ǣ���֪����ʹʯ��ˮ����ǵ��������ɣ�
��2�����ݼ���ʵ����֪���ᾧ��ֽ�ʱ��CO2�������ɣ����̽���ֽ����������CO����ʱ������Ҫ�ų�CO2�ĸ��ţ�������CO�Ļ�ԭ������������������֤��
��� �⣺��1�����Թ���ľ������ʱ��Ϊ��ֹ��Ӧ���ɵ�ˮ�������ᾧˮ�ڹܿ�Һ�����������Թ����ѣ�Ҫ���Թܿ�Ҫ������б��ʵ���������������ɣ����ܿ�������ð��������ʯ��ˮ����ǣ�֤����CO2�������ɣ��ʴ�Ϊ��û�������ܿ�������ð��������ʯ��ˮ����ǣ�CO2��
��2����Ϊ��֤�ֽ��������CO����Ҫ�ų���֤�����ɵ�CO2��ʵ��ĸ��ţ�����Fװ������CO2���壬������Dװ��֤��CO2�Ѿ��������ٽ��CO�Ļ�ԭ�ԣ���D���ų������徭G�����ͨ��Hװ���м��ȵ�����ͭ������Dװ����֤CO������������CO2����֤��CO�Ĵ��ڣ�����ٽ���β������������װ�õ�����˳��ΪA��B��F��D��G��H��D��I���ʴ�Ϊ��F��D��H��D������ͭ��
������Ӧ��������CO��ͨ���ų�CO2�ĸ��ź�������ʵ������ɹ۲쵽ͨHǰ��Dװ�ò������֤����CO2��H�к�ɫ��ĩ��Ϊ��ɫ֤���л�ԭ�����壬H�����Dװ���г���ʯ��ˮ�����֤����CO2���ɣ��ʴ�Ϊ��H֮ǰ��Dװ���г���ʯ��ˮ������ǣ�H�к�ɫ��ĩ��Ϊ��ɫ��H֮���Dװ���г���ʯ��ˮ����ǣ�
���� ʵ��̽���⣬����������ijɷݼ������漰CO��CO2�����ʣ��е��Ѷȣ�

��ʹ������ƿǰ����Ƿ�©ˮ����������ƿ���ܽ��������ƹ��壻
������ƿ������ˮϴ�����������ˮ��ʹ�ã�����Һ����ȴ�����·���ע������ƿ���ݼ�ˮ����ʱ����С�ij����̶��ߣ��õι���������Һ�壮
| A�� | �٢ڢ� | B�� | �٢ۢ� | C�� | �ۢܢ� | D�� | �٢ܢ� |
| A�� | ��������ģ��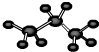 | B�� | N2�ĵ���ʽ 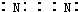 | ||
| C�� | ����ĽṹʽΪCH4 | D�� | ����ķ���ʽ CH3CH3 |
������������Ŀ֮��Ϊ7��11 ��������ԭ����Ŀ֮��Ϊ11��14
����ͬ���������֮��Ϊ11��7 ����ͬ�������ܶ�ֵ��Ϊ11��7��
| A�� | �ٺ͢� | B�� | �ں͢� | C�� | �ۺ͢� | D�� | �ں͢� |
| A�� | �������ڷ�Ӧ�еõ��ĵ���Խ�࣬��������Խǿ | |
| B�� | Cl2�ȿ��������������ֿ�����ԭ�� | |
| C�� | Cu2+�������Ա�Fe2+ǿ | |
| D�� | ��������ԭ��Ӧ�У��������õ��ĵ�������һ�����ڻ�ԭ��ʧȥ�ĵ������� |
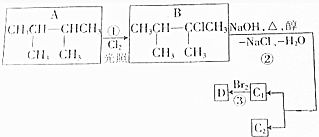
 ��
��