题目内容
13.下列可以大量共存且溶液是无色的离子组是( )| A. | Ba2+、Ca2+、OH-、HCO3- | B. | H+、K+、NH4+、SO42- | ||
| C. | NO3-、SO42-、K+、Mg2+ | D. | H+、Na+、NO3-、Cu2+ |
分析 根据离子之间不能结合生成沉淀、气体、水等,则离子大量共存,并结合常见离子的颜色来解答.
解答 解:A.Ca2+、OH-、HCO3-结合生成沉淀和水,Ba2+、OH-、HCO3-结合生成沉淀和水,不能大量共存,故A错误;
B.该组离子之间不反应,可大量共存,且离子均为无色,故B正确;
C.该组离子之间不反应,可大量共存,且离子均为无色,故C正确;
D.该组离子之间不反应,可大量共存,但Cu2+为蓝色,与无色不符,故D错误;
故选BC.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,注意常见离子的颜色,题目难度不大.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案
相关题目
3.下列烃在光照下与氯气反应,生成三种一氯代物的有( )
| A. | 2-甲基丙烷 | B. | 异戊烷 | C. | 2,2-二甲基丁烷 | D. | 2,3-二甲基丁烷 |
8.亚运期间,一些易燃、易爆、剧毒品、易腐蚀品等,严禁旅客带上车.下列化学药品,不允许旅客带上车的有
①浓硫酸②氰化钾③水银④TNT炸药⑤汽油⑥白磷( )
①浓硫酸②氰化钾③水银④TNT炸药⑤汽油⑥白磷( )
| A. | 只有①②④⑤⑥ | B. | 只有①②③④ | C. | 只有①②④ | D. | 都不行 |
7.对照元素周期表,下列叙述中不正确的是( )
| A. | 在过渡元素中可以寻找制备催化剂及耐高温和耐腐蚀合金材料的元素 | |
| B. | 在金属元素区域可以寻找制备新型农药材料的元素 | |
| C. | 在地球上元素的分布和它们在元素周期表中的位置有密切关系 | |
| D. | 在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素 |
8.下列说法正确的是( )
| A. | Li是最活泼金属,F是最活泼非金属 | |
| B. | Mg(OH)2碱性比Ca(OH)2强 | |
| C. | 元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共16纵行 | |
| D. | X2+的核外电子数目为10,则X在第3周期第ⅡA族 |
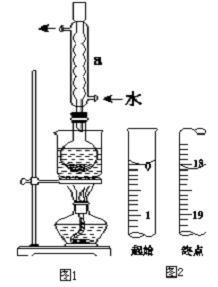 Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定.
Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定.