题目内容
【题目】Mg﹣H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液(加入一定量酸),示意图如图.该电池工作时,下列说法正确的是( ) 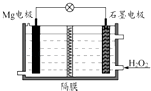
A.电池工作时,石墨周围海水的pH减少
B.电池工作时,溶液中的H+向负极移动
C.电池总反应为Mg+H2O2+2H+═Mg2++2H2O
D.Mg电极是该电池的正极
【答案】C
【解析】解:A.工作时,正极反应式为H2O2+2H++2e﹣═2H2O,不断消耗H+离子,正极周围海水的pH增大,故A错误;B.原电池中,阳离子向正极移动,阴离子向负极移动,形成闭合回路,所以溶液中的H+向正极移动,故B错误;
C.镁﹣﹣H2O2酸性电池的最终反应物为Mg2+和H2O,电池总反应式为Mg+H2O2+2H+=Mg2++2H2O,则电池总反应应为Mg+H2O2+2H+═Mg2++2H2O,故C正确;
D.组成的原电池的负极被氧化,镁为负极,而非正极,故D错误
故选C.

练习册系列答案
相关题目