题目内容
【题目】有机物与人们的衣、食、住、行及健康等有非常密切的关系,认知和研究有机物具有十分重要的作用.
(1)有机物A是构成营养素的基础物质(含C、O、H、N等元素),A的球棍模型如图所示,图中“棍”代表单键或双键或三键,不同颜色的球代表不同元素的原子.回答下列问题: A的分子式是 , 含氧官能团的名称是;
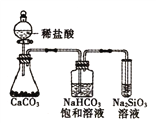
(2)将含有C、H、O的有机物3.24g装入元素分析装置,通入足量的O2使之完全燃烧,将生成的气体依次通过CaCl2管(A)和碱石灰(B),测得A管质量增加了2.16g,B管增加了9.24g,已知该有机物的相对分子质量为108. 该有机物的分子式为 , 该有机物1分子中有1个苯环,试写出它的同分异构体的结构简式中的任意一种 . 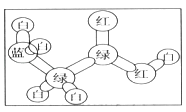
【答案】
(1)C2H5O2N;羧基
(2)C7H8O; 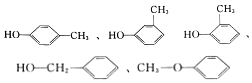 (任写一种)
(任写一种)
【解析】解:(1)根据原子成键特点知,蓝色球表示N原子、绿色球表示C原子、白色球表示H原子、红色球表示O原子,所以该分子结构简式为NH2CH2COOH,根据结构简式确定分子式为C2H5O2N,含氧官能团名称为羧基,
所以答案是:C2H5O2N;羧基;(2)该有机物完全燃烧后生成二氧化碳和水,氯化钙吸收的是水蒸气,然后碱石灰吸收的是二氧化碳,根据A管质量知,m(H2O)=2.16g,则n(H)= ![]() ×2=0.24mol,B管质量中m(CO2)=9.24g,n(C)=
×2=0.24mol,B管质量中m(CO2)=9.24g,n(C)= ![]() ×1=0.21mol,n(O)=
×1=0.21mol,n(O)= ![]() =0.03mol,
=0.03mol,
有机物的物质的量= ![]() =0.03mol,所以该有机物中C、H、O原子个数分别为
=0.03mol,所以该有机物中C、H、O原子个数分别为 ![]() =7、
=7、 ![]() =8、
=8、 ![]() =1,该分子式为C7H8O;
=1,该分子式为C7H8O;
该分子不饱和度= ![]() =4,苯环的不饱和度是4,所以该分子中除了含有苯环外不含有双键、三键,因为含有一个O原子,所以存在的官能团可能是﹣OH或﹣O﹣,则其同分异构体为
=4,苯环的不饱和度是4,所以该分子中除了含有苯环外不含有双键、三键,因为含有一个O原子,所以存在的官能团可能是﹣OH或﹣O﹣,则其同分异构体为 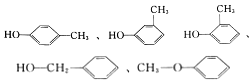 (任写一种),
(任写一种),
所以答案是:C7H8O;  (任写一种).
(任写一种).

 口算能手系列答案
口算能手系列答案【题目】煤的主要组成元素是碳、氢、氧、硫、氮,燃煤产生CxHy、SO2等大气污染物,煤的气化是高效、清洁利用煤炭的重要途径之一。回答下列问题:
(1)利用煤的气化获得的水煤气( 主要成分为CO、CO2和H2 )在催化剂作用下可以合成绿色燃料甲醇。
已知: H2O(1) = H2O(g) ΔH1= +44 .0kJ/mol
CO2(g)+H2(g) = CO(g)+H2O(g) ΔH2=-3.0kJ/mol
CO2(g)+3H2(g) = CH3OH(g)+H2O(g) ΔH3=-58.7 kJ/mol
写出由CO与H2制备CH3OH 气体的热化学方程式____________。
(2)甲醇和CO2可直接合成碳酸二甲酯(CH3OCOOCH3简称DMC) ;
2CH3OH(g)+CO2(g) ![]() CH3OCOOCH3(g)+H2O(g) ΔH4<0
CH3OCOOCH3(g)+H2O(g) ΔH4<0
①该化学反应的平衡常数表达式为K=__________
②在恒温恒容密闭容器中发生上述反应,能说明反应达到平衡状态的是________(填编号)。
A.V正(CH3OH)= 2V逆(H2O)
B.容器内气体的密度不变
C.容器内压强不变
D.CH3OH与CO2的物质的量之比保持不变
③一定条件下分别向甲,乙、丙三个恒容密闭容器中加入一定量的初始物质发生该反应,各容器中温度、反应物的起始量如下表,反应过程中DMC的物质的量浓度随时间变化如图所示:
容器 | 甲 | 乙 | 丙 |
容积(L) | 0.5 | 0.5 | V |
温度(℃) | T1 | T2 | T3 |
起始量 | 1molCO2(g) 2molCH3OH(g) | 1molDMC(g) 1molH2O(g) | 2molCO2(g) 2molCH3OH(g) |
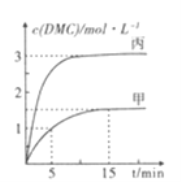
甲容器中,在5-15min时的平均反应速率v(CO2)=___________.乙容器中,若平衡时n(CO2)=0.2mol.则T1_____T2 (填“>”“<”或“=”)。两容器的反应达平衡时CO2的转化率: 甲________丙(填“>”“<."或”=”)。
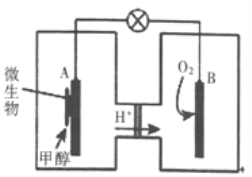
(3)利用甲醇可制成微生物燃料电池(利用微生物将化学能直接转化成电能的装置)。某微生物燃料电池装置如图所示: A极是_____极(填“正”或“负”),其电极反应式是_______。该电池不能在高温下工作的理由是________。