题目内容
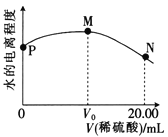
【题目】298K时,用0.1000mol·L-1稀硫酸滴定20.00mL 0.1000mol·L-1氨水,溶液中水的电离程度随所加稀硫酸体积的变化如图所示。下列说法不正确的是
A. 该实验可选择甲基橙作指示剂
B. 从P点到N点,溶液中水的电离程度先增大后减小
C. M点对应的溶液中:c(H+)=c(OH-)+c(NH3·H2O)
D. N点对应的溶液中:c(NH4+)+c(NH3·H2O)=2c(SO42-)
【答案】D
【解析】A、终点时,产物为硫酸铵,水解后呈酸性,可选用变色范围在酸性的指示剂,该实验可选择甲基橙作指示剂,故A正确;B、从P点到M点,碱性逐渐减弱,溶液中水的电离程度增大,从M点到N点,溶液中水的电离程度减小,故B正确;C、M点产物为硫酸铵,对应的溶液中存在质子守恒:c(H+)=c(OH-)+c(NH3·H2O),故C正确;D、N点相当于是硫酸和硫酸等物质的量混合形成的溶液,N原子与S原子比为1:1,对应的溶液中物料守恒的式子为:c(NH4+)+c(NH3·H2O)=c(SO42-),故D错误;故选D。

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
