题目内容
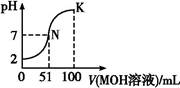
常温下,向100 mL 0.01 mol·L-1 HA溶液中逐滴加入0.02 mol·L-1 MOH溶液,图中所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中,正确的是( )

| A.HA可能为一元弱酸 |
| B.MOH为一元强碱 |
| C.N点水的电离程度小于K点水的电离程度 |
| D.若K点对应的溶液的pH=10,则有c(MOH)+c(M+)="0.01" mol·L-1 |
D
由图可知,常温下0.01 mol·L-1 HA溶液pH=2,则说明HA为一元强酸,A错;向100 mL 0.01 mol·L-1 HA溶液中逐滴加入0.02 mol·L-1 MOH溶液50 mL时,两者恰好反应生成盐,但溶液pH<7,溶液显酸性,故MOH为一元弱碱,B错;溶液中的MOH在K点比N点多了49 mL,c(OH-)大,抑制了水的电离,故N点水的电离程度大于K点,C错;K点溶液的体积为200 mL,根据物料守恒,c(MOH)+c(M+)= ="0.01" mol·L-1,D对。
="0.01" mol·L-1,D对。
 ="0.01" mol·L-1,D对。
="0.01" mol·L-1,D对。
练习册系列答案
相关题目



 >1
>1