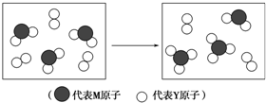
题目内容
7.“富勒烯”家族又增添了新成员,继C60、C90、N60之后,中美科学家首次发现了全硼富勒烯B60,下列说法正确的是( )| A. | B60和C90都属于新型化合物 | B. | C60和N60属于同分异构体 | ||
| C. | B60、C60、C90、N60都只含共价键 | D. | B60、C60、C90、N60都属于烯烃 |
分析 A.均只有一种元素组成,属于单质;
B.均为单质,且为不同元素的单质;
C.均只有一种元素,则只含非金属元素之间的化学键;
D.烯烃含C、H元素.
解答 解:A.B40和C70都只有一种元素组成,均属于单质,故A错误;
B.C60和N60为不同的单质,故B错误;
C.均只有一种元素,则只含非金属元素之间的化学键,则只含共价键,故C正确;
D.烯烃含C、H元素,几种单质均不含有H元素,不属于烯烃,故D错误;
故选C.
点评 本题考查化学键,为高频考点,把握物质的组成、相关概念的辨析、化学键的形成为解答的关键,侧重分析与迁移应用能力的考查,题目难度不大.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
17.下列说法中正确的是( )
| A. | 形成离子键的阴、阳离子间只存在静电吸引力 | |
| B. | 核外电子排布相同的微粒,化学性质相同 | |
| C. | 所有物质中均存在化学键 | |
| D. | 离子化合物中一定含有离子键 |
2.根据下表中的信息回答问题:
(1)B的原子结构示意图为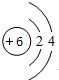 ,物质X的化学式为SiO2
,物质X的化学式为SiO2
(2)C、D、F三种元素对应的氢化物稳定性大小顺序是H2O>NH3>SiH4(填化学式)
(3)A、D、E三种元素形成的化合物中存在的化学键类型是离子键、共价键
(4)有两种盐,它们均由A、D、E、G四种元素组成,二者在溶液中反应的离子方程式是H++HSO3-=SO2↑+H2O
(5)B、F两元素中非金属性较强的是碳(写出元素名称),请设计一个简单的实验证明这一结论取硅酸钠溶液于试管中,向其中通入二氧化碳气体,观察是否有白色沉淀产生.
| Ⅰ | A、B、C、D、E、F、G七种短周期元素的原子序数依次增大 |
| Ⅱ | A和E同主族,B和F同主族,D和G同主族 |
| Ⅲ | A原子核内只有质子没有中子,B原子最外层电子数是电子层数的2倍 |
| Ⅳ | D和F以原子个数比为2:1组成的物质X是光导纤维的主要成分 |
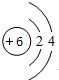 ,物质X的化学式为SiO2
,物质X的化学式为SiO2(2)C、D、F三种元素对应的氢化物稳定性大小顺序是H2O>NH3>SiH4(填化学式)
(3)A、D、E三种元素形成的化合物中存在的化学键类型是离子键、共价键
(4)有两种盐,它们均由A、D、E、G四种元素组成,二者在溶液中反应的离子方程式是H++HSO3-=SO2↑+H2O
(5)B、F两元素中非金属性较强的是碳(写出元素名称),请设计一个简单的实验证明这一结论取硅酸钠溶液于试管中,向其中通入二氧化碳气体,观察是否有白色沉淀产生.
12.下列关于氨气的说法不正确的是( )
| A. | 氨气极易溶于水 | B. | 氨的催化氧化可生成NO | ||
| C. | 氨气可用浓硫酸干燥 | D. | 氨气为无色有刺激性气味的气体 |
17.下列反应的离子方程式书写正确的是( )
| A. | 向稀硫酸中加入氢氧化钡溶液:OH-+H+═H2O | |
| B. | 铜与稀硝酸反应:Cu+2NO3-+4H+═Cu2++2NO2↑+2H2O | |
| C. | 向氯化铝溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| D. | 向氯化铁溶液中加入过量铜:Fe3++Cu═Fe+Cu2+ |
 某学习小组针对化学能转变为其他形式的能量,进行如下实验:
某学习小组针对化学能转变为其他形式的能量,进行如下实验: .
.