题目内容
【题目】下列组成生物体的化学元素中属于微量元素的一组是
A. H、N、P、Mn、C
B. Cl、Fe、S、N、Mg
C. Cu、Zn、Mn、Mo、B
D. Fe、N、P、K、Cu、I
【答案】C
【解析】试题解析:H、N、P、C属于大量元素,A不正确; Cl、S、N、Mg属于大量元素,B不正确;Cu、Zn、Mn、Mo、 B,均为微量元素,C正确;N、P、K属于大量元素,D不正确。

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
【题目】
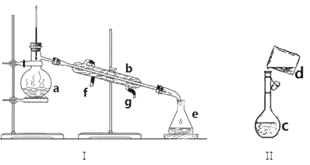
(1)写出下列仪器的名称:
a. b. c. e.
(2)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器是 。冷凝水由 (填f或g)口通入。
(3)现需配制0.1mol/LNaOH溶液450mL,装置II是某同学转移溶液的示意图。
①图中的错误是 。
②根据计算得知,用托盘天平所需称量NaOH的质量为 g。
③配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次)________。
A.用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶 |
B.称量计算出的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解并冷却至室温 |
C.将溶解的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中 |
D.将容量瓶盖紧,振荡,摇匀 |
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度2~3cm处
(4)物质的量浓度误差分析:(填偏高、偏低、无影响)
①用滤纸称量氢氧化钠 ;
②定容时,若眼睛俯视刻度线,则所配制的溶液浓度将 ;
③未冷却到室温就注入容量瓶定容 ;
④配好的溶液转入干净的试剂瓶时,不慎溅出部分溶液 。