题目内容
(10分)质量为34 g的NH3其物质的量是 mol,在标准状况下的体积约为 L 。0.1 mol H2S中有约 个氢原子;相同质量的NH3和H2S中分子个数比为 。配制100 mL浓度为1 mol·L-1的稀硫酸,需要用98%密度为1.84 g/cm3的浓硫酸 mL。
2; 44.8; 1.204×1023; 2:1; 5.4(各2分,共10分)
试题分析:(1)根据n=m/M可知,34g氨气的物质的量是34g÷17g/mol=2mol;在标准状况下的体积是V=2mol×22.4L/mol=44.8L;根据H2S的化学式可知,1个H2S分子中含有2个氢原子,所以0.1molH2S分子中含有0.2mol氢原子,其个数是0.2mol×6.02×1023/mol=1.204×1023;氨气和H2S的相对分子质量分别是17和34,所以在质量相等的条件下,二者的分子数之比是1/17︰1、34=2︰1;在稀释过程中溶质的质量是不变的,所以需要浓硫酸的体积是
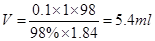 。
。点评:在进行物质的量的有关计算时,关键是熟练应用几个关系式
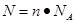 、n=m/M、
、n=m/M、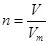 、
、 ,特别还要注意气体摩尔体积的使用条件,即只能适用于气体,且只有在标准状况下,气体的摩尔体积才是22.4L/mol。例外还需要注意分子的个数和原子的个数是不同的,计算时需要分清楚。
,特别还要注意气体摩尔体积的使用条件,即只能适用于气体,且只有在标准状况下,气体的摩尔体积才是22.4L/mol。例外还需要注意分子的个数和原子的个数是不同的,计算时需要分清楚。
练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目
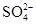 的物质的量浓度是 。
的物质的量浓度是 。