题目内容
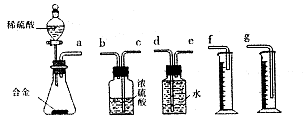
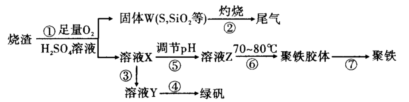
绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的重要成分。下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:
查询资料,得有关物质的数据如下表:
| 25℃时 | pH值 |
| 饱和H2S溶液 | 3.9 |
| SnS沉淀完全 | 1.6 |
| FeS开始沉淀 | 3.0 |
| FeS沉淀完全 | 5.5 |
(1)检验制得的绿矾晶体中是否含有Fe3+,最好选用的试剂为 。
A.KSCN溶液 B.NaOH溶液 C.KMnO4溶液 D.苯酚溶液
(2)操作II中,通入硫化氢至饱和的目的是 ;在溶液中用硫酸酸化至pH=2的目的是 。
(3)操作IV的顺序依次为 、冷却结晶、 。
(4)操作IV得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质;② 。
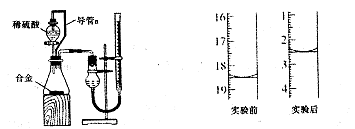
(5)测定绿矾产品中Fe2+含量的方法是:a.称取2.850g绿矾产品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测溶液于锥形瓶中;c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。
①滴定时盛放KMnO4溶液的仪器为 (填仪器名称)。
②判断此滴定实验达到终点的方法是 。
③计算上述样品中FeSO4·7H2O的质量分数为 。
解析试题分析:(1)检验Fe3+通常用KSCN溶液,加入KSCN溶液,溶液显血红色;Fe3+加入苯酚溶液,溶液显紫色,据此也可检验Fe3+。
(2)通入H2S可以使Sn2+完全沉淀,S2-具有还原性,还可以防止Fe2+被氧化。根据题中数据,将溶液酸化至pH=2,目的是只沉淀Sn2+,防止Fe2+沉淀。
(3)从溶液中得到晶体的操作一般为蒸发浓缩、冷却结晶、过滤洗涤。
(4)用冰水洗涤一方面可以出去杂质,另一方面降低FeSO4·7H2O的溶解度,减小洗涤过程中的损失。
(5)①盛放酸性高锰酸钾溶液应用酸式滴定管。
②高锰酸钾溶液有颜色,滴入最后一滴时,溶液显浅红色,且半分钟不褪色,则达到终点。
③根据关系式5Fe2+~KMnO4,可知样品中所含FeSO4·7H2O的物质的量为0.01000mol/L×0.02L×5×10=0.01mol,故样品中FeSO4·7H2O的质量分数为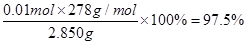 。
。
考点:考查工艺流程,离子检验,实验基础操作,中和滴定,化学计算等。

FeCl3在现代工业生产中应用广泛。某化学研究性学习小组模拟工业生产流程制备无水FeCl3,再用副产品FeCl3溶液吸收有毒的H2S。
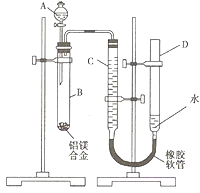
经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。他们设计了制备无水FeCl3的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下: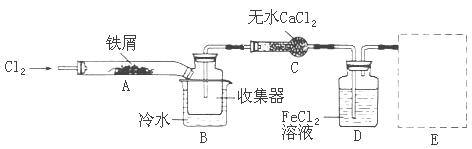
①检查装置的气密性;
②通入干燥的Cl2,赶尽装置中的空气;
③用酒精灯在铁屑下方加热至反应完成
④ ……
⑤体系冷却后,停止通入Cl2,并用干燥的N2赶尽Cl2,将收集器密封
请回答下列问题:
(1)写出FeCl3溶液吸收有毒的H2S的离子方程式为
(2)第③步加热后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管A的右端。要使沉积得FeCl3进入收集器,第④步操作是
(3)操作步骤中,为防止FeCl3潮解所采取的措施有(填步骤序号)
(4)装置B中的冷水作用为 ;装置C的名称为 ;装置D中FeCl2全部反应完后,因为失去吸收Cl2的作用而失效,从下面选出检验FeCl2是否完全失效的试剂:___
| A.氢氧化钠溶液 | B.酸性高锰酸钾溶液 | C.硫氰化钾溶液 | D.氨水 |
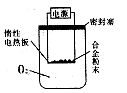
加热熔融烧碱时应使用下列哪种坩埚
| A.石英坩埚 | B.普通玻璃坩埚 | C.铁坩埚 | D.陶瓷坩埚 |

 。
。
 。
。