题目内容
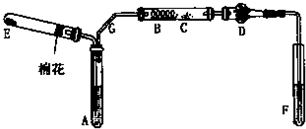
某实验兴趣小组设计如下微型实验装置。实验时,先断开S2,闭合S1,两极均有气泡产生;一段时间后,断开S1,闭合S2,发现电流表A的指针偏转,下列有关描述正确的是

A.断开S2闭合S1时,总反应的离子方程式为:2H++2Cl- H2↑+Cl2↑
H2↑+Cl2↑
B.断开S2闭合S1时,阳极附近溶液变红
C.断开S1闭合S2时,铜电极上的电极反应为:Cl2+2e→2Cl-
D.断开S1闭合S2时,石墨电极作正极
【答案】
D
【解析】
试题分析:A、断开S2,闭合S1时,是电解池装置,两极均有气泡产生,说明是电解饱和食盐水的反应,反应的离子方程式为2H2O+2Cl- Cl2↑+H2↑+2OH-;故A错误;B、断开S2,闭合S1时,是电解池装置,两极均有气泡产生,石墨做阳极,溶液中氯离子离子失电子发生氧化反应,铜做阴极,氢离子得到电子发生还原反应,依据水的电离平衡,氢氧根离子浓度增大酚酞变红;故B错误;C、断开S1,闭合S2时,发现电流表指针偏转,证明是原电池反应,形成氢氯燃料电池,铜做负极发生氢气失电子生成氢离子的反应;故C错误D、断开S1,闭合S2时,发现电流表指针偏转,证明是原电池反应,形成氢氯燃料电池,石墨做原电池正极;故D正确。
Cl2↑+H2↑+2OH-;故A错误;B、断开S2,闭合S1时,是电解池装置,两极均有气泡产生,石墨做阳极,溶液中氯离子离子失电子发生氧化反应,铜做阴极,氢离子得到电子发生还原反应,依据水的电离平衡,氢氧根离子浓度增大酚酞变红;故B错误;C、断开S1,闭合S2时,发现电流表指针偏转,证明是原电池反应,形成氢氯燃料电池,铜做负极发生氢气失电子生成氢离子的反应;故C错误D、断开S1,闭合S2时,发现电流表指针偏转,证明是原电池反应,形成氢氯燃料电池,石墨做原电池正极;故D正确。
考点:原电池和电解池的工作原理

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案
相关题目
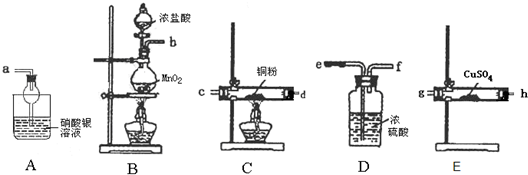
 如图是某化学兴趣小组设计的制取溴苯的实验装置,装置A是酸式滴定管,分液漏斗中是苯和液溴的混合物,打开分液漏斗的活塞,使混合物滴在铁丝上(酸式滴定管活塞关闭).试回答下面的问题:
如图是某化学兴趣小组设计的制取溴苯的实验装置,装置A是酸式滴定管,分液漏斗中是苯和液溴的混合物,打开分液漏斗的活塞,使混合物滴在铁丝上(酸式滴定管活塞关闭).试回答下面的问题:


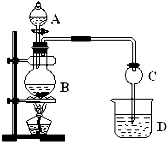 某化学兴趣小组设计实验制取乙酸乙酯.现用如图装置进行实验,在圆底烧瓶内加入碎瓷片,再加入由2mL 98%的浓H2SO4和3mL乙醇组成的混合液,通过分液漏斗向烧瓶内加入2mL冰醋酸,烧杯中加入饱和Na2CO3溶液.请回答下列问题:
某化学兴趣小组设计实验制取乙酸乙酯.现用如图装置进行实验,在圆底烧瓶内加入碎瓷片,再加入由2mL 98%的浓H2SO4和3mL乙醇组成的混合液,通过分液漏斗向烧瓶内加入2mL冰醋酸,烧杯中加入饱和Na2CO3溶液.请回答下列问题: