题目内容
【题目】三氧化二镍是一种重要的电子元件材料、蓄电池材料。工业上利用含镍废料(以镍铁、钙、镁合金为主)制取草酸镍(NiC2O4·2H2O),再高温煅烧草酸镍制取三氧化二镍。已知草酸的钙、镁、镍盐均难溶于水。根据下列工艺流程示意图回答问题。
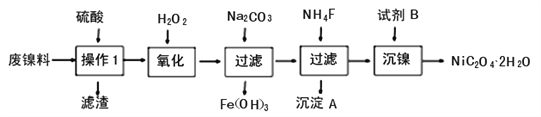
(1)操作1的名称为________________。
(2)沉淀A为______________________________(用电子式表示)。
(3)试剂B的名称为____________________________,沉镍后,滤液中C2O42-的浓度为0.01mol/L,则残留在滤液中的 c(Ni2+)=_______________(已知Ksp[NiC2O4]= 4×10-10)。
(4)NiC2O4·2H2O 高温煅烧制取三氧化二镍的热重曲线如图所示:

①T3温度后,草酸镍全部转化为三氧化二镍,则a为____________(保留一位小数)。
②T2温度发生反应的化学方程式为________________________。
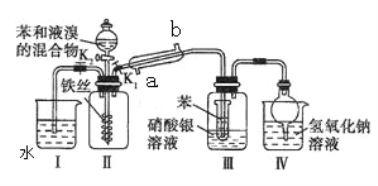
(5)高温煅烧草酸镍制取三氧化二镍时会产生CO、CO2、水蒸气等混合气体。某同学设计如下实验流程进行检验。
混合气体![]() 现象
现象![]() 澄清石灰水变浑浊
澄清石灰水变浑浊
①试剂1的化学式为____________________。
②碱石灰的作用是_____________________________________。
【答案】 过滤 ![]() 、
、![]() 草酸或可溶性的草酸盐 4×10-8mol/L 45.4 NiC2O4·H2O
草酸或可溶性的草酸盐 4×10-8mol/L 45.4 NiC2O4·H2O![]() NiC2O4 +H2O CuSO4 吸收二氧化碳,避免对CO的检验产生干扰
NiC2O4 +H2O CuSO4 吸收二氧化碳,避免对CO的检验产生干扰
【解析】(1)根据流程图,操作1是过滤操作;
(2)分析框图:“酸溶”生成含镍、铁、钙、镁离子的溶液,加双氧水的目的是氧化生成Fe3+,加入碳酸钠溶液的作用是调节pH,促进铁离子水解沉淀完全,再加入NH4F的目的是除去钙离子、镁离子;(3)加入试剂B是生成草酸镍;根据Ksp[NiC2O4]= 4×10-10计算c(Ni2+);(4)①T3温度后,草酸镍全部转化为三氧化二镍,根据关系式2NiC2O4·2H2O~ Ni2O3计算a。
②根据![]() 失去9.8%的质量,183
失去9.8%的质量,183![]()
![]() 18,恰好是失掉1分子水,
18,恰好是失掉1分子水,![]() 失去9.9%的质量,183
失去9.9%的质量,183![]()
![]() 18,失掉另1分子水;
18,失掉另1分子水;
(5)检验CO、CO2、水蒸气等混合气体先用无水硫酸铜检验水蒸气,再用澄清石灰水检验二氧化碳,再用碱石灰除去二氧化碳和水蒸气,再用灼热氧化铜检验CO;最后把气体通入澄清石灰水。
解析:(1)根据流程图,操作1实现固体与液体分离是过滤操作;
(2)分析框图:“酸溶”生成含镍、铁、钙、镁离子的溶液,加双氧水的目的是氧化生成Fe3+,加入碳酸钠溶液的作用是调节pH,促进铁离子水解沉淀完全,再加入NH4F的目的是除去钙离子、镁离子,所以加入氟化铵产生氟化钙、氟化镁沉淀,电子式为![]() 、
、![]() ;(3)加入试剂B是生成草酸镍,所以试剂B是草酸或可溶性的草酸盐;根据Ksp[NiC2O4]= 4×10-10,c(Ni2+)=
;(3)加入试剂B是生成草酸镍,所以试剂B是草酸或可溶性的草酸盐;根据Ksp[NiC2O4]= 4×10-10,c(Ni2+)=![]() 4×10-8mol/L;(4)①T3温度后,草酸镍全部转化为三氧化二镍,根据关系式
4×10-8mol/L;(4)①T3温度后,草酸镍全部转化为三氧化二镍,根据关系式
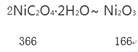 ,a=45.4%
,a=45.4%
②根据![]() 失去9.8%的质量,183
失去9.8%的质量,183![]()
![]() 18,恰好是失掉1分子水,
18,恰好是失掉1分子水,![]() 失去9.9%的质量,183
失去9.9%的质量,183![]()
![]() 18,失掉另1分子水;
18,失掉另1分子水;![]() 发生反应的方程式为NiC2O4·H2O
发生反应的方程式为NiC2O4·H2O![]() NiC2O4 +H2O;
NiC2O4 +H2O;
(5)根据以上分析①试剂1的化学式为CuSO4。
②碱石灰的作用是吸收二氧化碳,避免对CO的检验产生干扰;