题目内容
3.将一个容积为1L的密闭容器中放入2 mol SO2和1 mol O2,在一定的条件下,2s末测得容器内有0.8 mol SO2,求2s内SO2、O2、SO3的平均反应速率和反应速率比.分析 2s末测得容器内有0.8 mol SO2,则v(SO2)=$\frac{\frac{2mol-0.8mol}{1L}}{2s}$=0.6mol/(L.s),发生2SO2+O2=2SO3,结合反应速率之比等于化学计量数之比解答.
解答 解:2s末测得容器内有0.8 mol SO2,则v(SO2)=$\frac{\frac{2mol-0.8mol}{1L}}{2s}$=0.6mol/(L.s),
由反应速率之比等于化学计量数之比可知,v(SO3)=0.6mol/(L.s),
v(O2)=0.6mol/(L.s)×$\frac{1}{2}$=0.3mol/(L.s),
SO2、O2、SO3的反应速率比为2:1:2,
答:SO2、O2、SO3的平均反应速率分别为0.6mol/(L.s)、0.3mol/(L.s)、0.6mol/(L.s),反应速率比为2:1:2.
点评 本题考查化学反应速率的计算,为高频考点,把握速率计算公式及反应速率与化学计量数的关系为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
相关题目
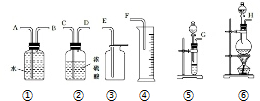
13.卤代烃R-CH2-CH2-X中的化学键如图所示,则下列说法正确的是( )


| A. | 发生水解反应时,被破坏的键是①和③ | |
| B. | 发生消去反应时,被破坏的键是①和③ | |
| C. | 发生水解反应时,被破坏的键是① | |
| D. | 发生消去反应时,被破坏的键是①和② |
11.单质X和单质Y能发生下列化学反应,每一个反应只有两种元素的化合价发生了变化:
①X+H2O→W+H2
②Y+H2O→N+O2
下列说法正确的是( )
①X+H2O→W+H2
②Y+H2O→N+O2
下列说法正确的是( )
| A. | X一定是非金属单质 | B. | X一定是金属单质 | ||
| C. | Y一定是非金属单质 | D. | Y一定是金属单质 |
 现有一定量的乙醚和乙醇的混合物试样.请从图中选用适当的实验装置,设计一个最简单的实验,测定试样中乙醇的含量.可供选用的反应物和试剂为:新制的生石灰、浓硫酸、蒸馏水、金属钠、碱石灰、无水硫酸铜.
现有一定量的乙醚和乙醇的混合物试样.请从图中选用适当的实验装置,设计一个最简单的实验,测定试样中乙醇的含量.可供选用的反应物和试剂为:新制的生石灰、浓硫酸、蒸馏水、金属钠、碱石灰、无水硫酸铜.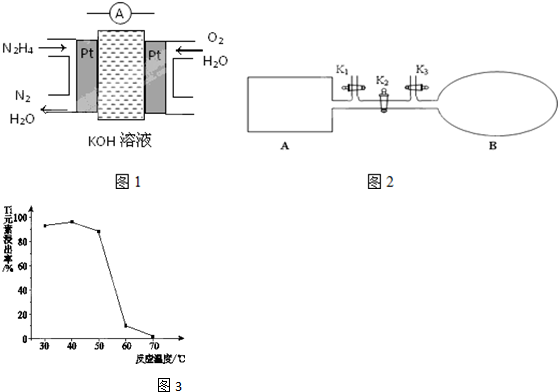
 .
.