题目内容
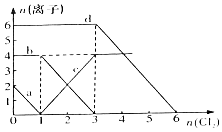
【题目】如图装置,将溶液A逐滴加入固体B中,下列叙述中不正确的是( ) 
A.若A为浓盐酸,B为MnO2 , C中盛品红溶液,则C中溶液不褪色
B.若A为醋酸溶液,B为贝壳,C中盛过量澄清石灰水,则C中溶液变浑浊
C.若A为浓硫酸,B为Na2SO3固体,C中盛石蕊溶液,则C中溶液先变红后褪色
D.若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中产生白色沉淀
【答案】C
【解析】解:A.二氧化锰(MnO2)与浓盐酸混合加热可得到氯气,反应方程式为:MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,而题目中的装置制取气体无需加热,所以无法制取氯气,C中盛品红溶液,则C中溶液无法褪色,故A正确;
MnCl2+Cl2↑+2H2O,而题目中的装置制取气体无需加热,所以无法制取氯气,C中盛品红溶液,则C中溶液无法褪色,故A正确;
B.贝壳的主要成分为碳酸钙,醋酸和碳酸钙反应CaCO3+2CH3COOH=Ca(CH3COO)2+H2O+CO2↑生成二氧化碳无需加热,二氧化碳和澄清石灰水反应CO2+Ca(OH)2═CaCO3↓+H2O生成不溶于水的碳酸钙,所以试管中溶液变浑浊,故B正确;
C.亚硫酸是弱酸,硫酸是强酸,利用强酸制弱酸的原理,强酸硫酸和亚硫酸钠反应生成弱酸亚硫酸,亚硫酸分解生成二氧化硫和水,Na2SO3+H2SO4═Na2SO4+SO2↑+H2O,所以能用图中左图的制取装置制备SO2 , 二氧化硫溶于水反应生成亚硫酸,能使C中盛石蕊试液变红,但不能漂白,所以不褪色,故C错误;
D.实验室制备NH3 , 可用浓氨水和CaO固体反应,NH3H2O+CaO═Ca(OH)2+NH3↑,浓氨水易挥发,CaO固体与水反应放出大量的热,导致温度升高,使得氨气在水中的溶解度进一步减少,以气体的形式逸出,制得氨气,可选择图中左图的制取装置,C中盛AlCl3溶液,氨气和水反应生成氨水,氨水和AlCl3溶液反应生成氢氧化铝沉淀,但氨水是弱碱,不能溶解氢氧化铝,故D正确;
故选C.
根据装置图可知,该装置适用于固体和液体无需加热制取气体,制取的气体易溶于试管中的液体,据此对照各选项进行分析即可解答.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某研究性学习小组通过下列反应原理制备SO2并进行性质探究.反应原理为:Na2SO3(固)+H2SO4(浓)=Na2SO4+SO2↑+H2O 
(1)根据上述原理制备并收集干燥SO2的实验装置连接顺序为 .
(2)D中盛装的试剂为 .
(3)甲同学用注射器吸取纯净的SO2并结合装置G进行SO2的性质实验,若X是Na2S溶液,其目的是检验SO2的 , 可观察到的现象 .
(4)实验1:乙同学将溶液X换为浓度均为0.1mol/L Fe(NO3)3和BaCl2的混合溶液(已经除去溶解氧),通入少量SO2后观察到烧杯产生白色沉淀,乙同学认为白色沉淀为BaSO4 , 为探究白色沉淀的成因,他继续进行如下实验验证:(已知:0.1mol/L Fe(NO3) 3的pH=2)
实验 | 操作 | 现象 | 结论和解释 |
2 | 将SO2通入0.1mol/L和BaCl2混合液 | 产生白色沉淀 | Fe3+能氧化H2SO3 |
3 | 将SO2通入和 BaCl2混合液 | 产生白色沉淀 | 酸性条件NO3﹣能将H2SO3氧化为SO42﹣ |
(5)丙同学认为以上实验只能说明Fe3+和酸性条件下NO3﹣均能将H2SO3氧化为SO42﹣ , 不能说明谁先氧化H2SO3 , 他利用提供的试剂(限选试剂:KSCN溶液,K3[Fe(CN)6]溶液,苯酚溶液,硝酸溶液)设计实验方案探究何种微粒先发生反应.请帮助他完成方案(包括操作现象和结论):取乙同学实验1后装置G中烧杯的上层清液于试管中, .
(6)丁同学在实验2过程发现,黄色溶液先变红棕色后慢慢变浅绿色,查阅资料得:Fe3++6SO2Fe(SO2)63+(红棕色).请用化学平衡移动原理解释实验2中溶液颜色变化的原因 .