题目内容
【题目】现有四种白色固体:①氯化钠②氯化钡③无水硫酸铜④硫酸钠,不使用其它试剂(可以用水)就可以把它们区分开,区分出的先后顺序是( )
A.②③④①B.②④③①C.③①④②D.③②④①
【答案】D
【解析】
将四种白色固体分别加入水,溶液为蓝色的是无水硫酸铜;将硫酸铜溶液分别于其他三种溶液混合,由于氯化钡溶液能与硫酸铜溶液产生白色沉淀,故产生白色沉淀的溶液是氯化钡溶液,其余两种为氯化钠和硫酸钠;然后将鉴别出来的氯化钡溶液与剩余两种溶液混合,氯化钡溶液能与硫酸钠溶液产生白色沉淀,故产生白色沉淀的是硫酸钠,另外一种是氯化钠,故鉴别出来的顺序是③②④①,观察选项,故答案选D。

 阅读快车系列答案
阅读快车系列答案【题目】“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视。所以“低碳经济”正成为科学家研究的主要课题。
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:
___ C+ ___ KMnO4+ H2SO4 = ____CO2↑+ ____MnSO4 + ____K2SO4+
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)![]() CO2(g)+H2(g),得到如下二组数据:
CO2(g)+H2(g),得到如下二组数据:
实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
CO | H2O | H2 | CO | |||
1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
①实验1中以CO2表示的化学反应速率为__________(保留小数点后二位数,下同)。
②实验2条件下平衡常数K=_________,该反应为 _____(填“吸”或“放”)热反应。
(3)已知在常温常压下:
① 2CH3OH(l)+3O2(g) = 2CO2(g)+4H2O(g) ΔH = -1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH = -566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH = -44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和气态水的热化学方程式:_____________。
(4)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置。
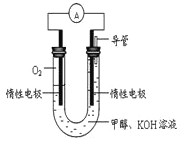
①该电池负极的电极反应为:_______________。
②该电池工作时,溶液中的OH-向______极移动。
【题目】已知H2(g)+Br2(g)===2HBr(g) ΔH=-72 kJ/mol,其他相关数据如下表:
物质 | H2(g) | Br2(g) | HBr(g) |
1 mol 分子中的化学键断 裂时需要吸收的能量/kJ | 436 | a | 369 |
则表中a为( )
A.404B.260C.230D.200