题目内容
下列说法中,正确的是( )
| A.CO2的摩尔质量是44 g |
| B.18 g H2O在标准状况下的体积是22.4 L |
| C.在标准状况下,20 mL NH3与60 mL O2所含的分子数比为1∶3。 |
| D.将40 g NaOH溶于1 L水中,所得溶液的物质的量浓度为1 mol/L |
C
解析试题分析:A、CO2的摩尔质量是44 g/mol,g是质量的单位,错误;B、H2O在标况下为液体,错误;C、氨气和氧气的体积之比为20∶60=1∶3,由阿伏加德罗定律推断,二者的物质的量之比为1∶3,正确;D、溶液的体积应为1L,而非水的体积为1L,错误。
考点:考查摩尔质量、质量、物质的量、气体摩尔体积、体积、微粒数、阿伏加德罗定律、物质的量浓度等相关知识。

练习册系列答案
相关题目
某结晶水合物的化学式为R?nH2O,其相对分子质量为M。25℃时,将a g该晶体溶于b g H2O中恰好形成V mL饱和溶液。下列表达式正确的是
A.饱和溶液物质的量浓度为: 1000 a(M -18n) mol/L 1000 a(M -18n) mol/L |
B.饱和溶液溶质的质量分数为: |
C.25℃时R的溶解度为: g/100 g H2O g/100 g H2O |
D.饱和溶液的密度为: g/mL g/mL |
下列化学用语正确的是( )
A.14C原子结构示意图: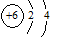 |
B.硝基苯的结构简式: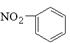 |
C.NH4Cl的电子式: |
| D.FeS2中S的化合价:?2 |
下列有关化学用语使用正确的是 ( )
A.HClO的电子式: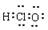 |
B.具有16个质子、16个中子和18个电子的微粒是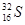 |
C.邻羟基苯甲酸的结构简式: |
D.乙烯的比例模型: |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.1 L 0.1 mol·L-1的氨水中含有的NH3·H2O分子数为0.1 NA |
| B.电解精炼铜时,若阳极质量减少6.4 g,则电路中转移电子数为0.2 NA |
| C.标准状况下,2.24 L的二氯甲烷中含有的碳氯共价键的数目为0.2 NA |
| D.一定条件下,4.6 g NO2和N2O4混合气体中含有的N原子数目为0.1 NA |
设NA表示阿伏加德罗常数的值。下列叙述不正确的是
| A.1 mol Na2O和Na2O2的混合物中含有的阴、阳离子总数是3NA |
| B.常温下,1 L 0.1 mol·L-1的NH4NO3溶液中含有的氮原子数为0.2NA |
| C.46 g有机物C2H6O中含有的H—O键的数目为NA |
| D.标准状况下,将0.1 mol Cl2通入足量NaOH溶液中,反应转移的电子数为0.1NA |
下列有关化学用语表示正确的是
A.Cl-的结构示意图: |
B.次氯酸的结构式: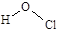 |
C.CH3F的电子式: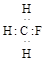 |
D.CO2的分子比例模型: |
设nA为阿伏加德罗常数的值,下列说法正确的是(相对原子质量:C-l2 H-1)
| A.2.24L NO2含有0.2nA个氧原子 |
| B.常温常压下,C2H4和C3H6组成的28g混合气体中含4nA个氢原子 |
| C.1 molC2H6分子中含有7nA个极性键 |
| D.常温下pH=13的NaOH溶液中含有的0.1 nA个OH- |
设NA为阿伏加德罗常数的值,下列叙述不正确的是( )
| A.常温常压下,17 g甲基(—14CH3)所含的中子数为8 NA |
| B.室温下,31.0g白磷中含有的共价键数目为1.5NA |
| C.标准状况下,44.8 L NO与22.4 LO2混合后气体中分子总数为2NA |
| D.1 molNa2O和Na2O2混合物中含有的阴、阳离子总数是3NA |