题目内容
4.分类是化学学习与研究的常用方法,下列分类正确的是( )| A. | Cl2O7、P2O5、SO3、CO2均属于酸性氧化物 | |
| B. | Na2O、Na2O2为相同元素组成的金属氧化物,都属于碱性氧化物 | |
| C. | 根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 | |
| D. | 根据溶液导电能力强弱,将电解质分为强电解质、弱电解质 |
分析 A、和碱反应生成盐和水的氧化物为酸性氧化物;
B.碱性氧化物是可以和酸之间反应生成盐和水的氧化物;
C.根据分散系中分散质粒子直径大小分类;
D、依据溶液中是否完全电离,电解质分为强电解质和弱电解质.
解答 解:A、和碱反应生成盐和水的氧化物为酸性氧化物,Cl2O7、P2O5、SO3、CO2均和碱反应生成盐和水属于酸性氧化物,故A正确;
B.氧化钠属于碱性氧化物,但是过氧化钠不是,故B错误;
C.根据分散系中分散质粒子直径大小将分散系分为溶液、胶体和浊液,故C错误;
D、依据溶液中是否完全电离,电解质分为强电解质和弱电解质,强电解质导电能力不一定比弱电解质,故D错误;
故选A.
点评 本题考查了化学概念的分析判断,概念的实质理解应用,分散系的分类,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
9.认真审题,完成下列实验探究.
(1)探究潮湿氯气与碳酸钠反应的产物
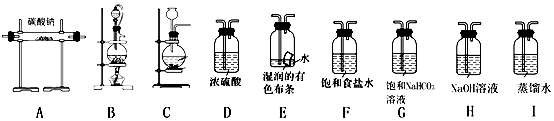
①选择必要的仪器,按BFAH顺序连接好装置(填装置序号).
②写出在该实验情境下,制备氯气的化学方程式MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
③将A中充分反应后的固体物质分成两等份分装于两支试管中.
向其中一支试管中加蒸馏水至固体完全溶解后,滴加BaCl2溶液,无明显现象,再滴加NaOH溶液变浑浊,由此现象推断固体产物中含有NaHCO3;向另一支试管中滴加过量的稀HNO3,再滴加AgNO3溶液,溶液变浑浊,由此现象推断固体产物中含有NaCl;
又已知A中反应还生成黄红色的Cl2O气体,请结合上述成分分析过程,写出潮湿的Cl2和Na2CO3的化学方程式2Cl2+2Na2CO3+H2O=2NaCl+2NaHCO3+Cl2O.
(2)二氧化碳与过氧化钠反应探究.
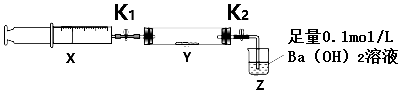
将一定量(过量)二氧化碳充入注射器X中,硬质玻璃管Y中加入少量过氧化钠,两端用夹子K1、K2夹好.在室温下按如图示装置进行实验.
(1)探究潮湿氯气与碳酸钠反应的产物

①选择必要的仪器,按BFAH顺序连接好装置(填装置序号).
②写出在该实验情境下,制备氯气的化学方程式MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
③将A中充分反应后的固体物质分成两等份分装于两支试管中.
向其中一支试管中加蒸馏水至固体完全溶解后,滴加BaCl2溶液,无明显现象,再滴加NaOH溶液变浑浊,由此现象推断固体产物中含有NaHCO3;向另一支试管中滴加过量的稀HNO3,再滴加AgNO3溶液,溶液变浑浊,由此现象推断固体产物中含有NaCl;
又已知A中反应还生成黄红色的Cl2O气体,请结合上述成分分析过程,写出潮湿的Cl2和Na2CO3的化学方程式2Cl2+2Na2CO3+H2O=2NaCl+2NaHCO3+Cl2O.
(2)二氧化碳与过氧化钠反应探究.
将一定量(过量)二氧化碳充入注射器X中,硬质玻璃管Y中加入少量过氧化钠,两端用夹子K1、K2夹好.在室温下按如图示装置进行实验.

| 操作步骤 | 实验现象 | 解释原因 |
| 打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中(假设充分反应) | ①淡黄色固体变为白色粉末 | ②反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2 |
| 将注射器活塞退回原处并固定,待装置恢复到室温,打开K2 | ③Z中液体出现倒吸 | ④不用解释 |
10.下列物质在水溶液中的电离方程式书写正确的是( )
| A. | KClO3═K++3O2-+Cl5+ | B. | NaHCO3═Na++H++CO32- | ||
| C. | H2SO4═H++SO42- | D. | Al2(SO4)3═2Al3++3SO42- |
12.下列实验操作能达到实验目的是( )
| A. | 用分液漏斗分离乙醇与油脂的混合物 | |
| B. | 用玻璃棒蘸取次氯酸溶液点在干燥的pH试纸中部,测定次氯酸溶液的pH | |
| C. | 在含FeCl3杂质的MgCl2溶液中加入适量的MgCO3,微热,充分搅拌,静置,过滤得较纯净的MgCl2溶液 | |
| D. | 将甲烷与氯气按物质的量之比1:2通入烧瓶,光照,制取纯净的CH2Cl2 |
19.将O2和NH3的混合气体448mL通过加热的三氧化二铬(催化剂),充分反应后,再通过足量的水,最终收集到44.8mL氧气.原混合气体中O2的体积可能是(假设氨全部被氧化;气体体积均已换算成标准状况)( )
已知:NO在 O2存在时与水可按4NO+3O2+2H2O=4HNO3反应进行.
已知:NO在 O2存在时与水可按4NO+3O2+2H2O=4HNO3反应进行.
| A. | 231.5mL | B. | 268.8mL | C. | 287.5mL | D. | 313.6mL |
9.用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 通常状况下,NA 个CO2分子占有的体积为22.4L | |
| B. | 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA | |
| C. | 标准状况下,22.4LH2O含有的分子数为 NA | |
| D. | 物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为NA |
13.下列说法不正确的是( )
| A. | 糖类和蛋白质都是人体重要的营养物质 | |
| B. | 蛋白质在一定条件下能发生水解反应,生成氨基酸 | |
| C. | 加热能杀死甲型H1N1流感病毒,因为病毒的蛋白质受热变性 | |
| D. | 蛋白质溶液中加入饱和硫酸铵溶液,蛋白质析出,如再加水也不溶解 |
14.据报道用Mg与作电极与NH4Cl溶液形成原电池,也可生成NH3.下列说法不正确的是( )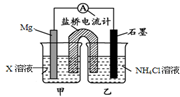

| A. | 盐桥中的K+移向乙烧杯 | |
| B. | 乙烧杯中一直存在:c(Cl-)>c(NH4+) | |
| C. | X可能是CuCl2 | |
| D. | 石墨电极反应式为2NH4++2e-═2NH3↑+H2↑ |