题目内容
13.下列反应中,属于取代反应的是( )| A. | CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O | B. | 2CH2CH2OH$→_{△}^{Cu}$2CH3CHO+H2O | ||
| C. | CH4+Cl2$\stackrel{光}{→}$CH2Cl+HCl | D. | CH2═CH2+H2$\stackrel{催化剂}{→}$CH3-CH3 |
分析 根据取代反应的定义“有机化合物分子里的某些原子或原子团被其它原子或原子团所代替的反应”进行判断.
解答 解:A.甲烷燃烧生成二氧化碳与水,属于氧化反应,故A错误;
B、乙醇在Cu的催化氧化下生成醛和水,属于氧化反应,故B错误;
C、甲烷和氯气在光照条件下发生反应属于取代反应,故C正确;
D、乙烯与氢气发生反应生成乙烷,属于加成反应,故D错误,
故选C.
点评 本题考查了取代反应、加成反应、氧化反应的判断,难度不大,正确理解概念是解本题的关键.

练习册系列答案
 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
1.下列说法中正确的是( )
| A. | 不管什么反应使用催化剂,都可以加快反应速率 | |
| B. | 可逆反应A(g)?B(g)+C(g),增大压强,正反应速率减小,逆反应速率增大 | |
| C. | 对达到平衡的一个放热的可逆反应,若降温,则正反应速率减小,逆反应速率增大 | |
| D. | 参加反应的物质的性质是决定化学反应速率的主要因素 |
8.X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族,其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9.单质Y和W都可与浓的NaOH溶液反应.下列说法不正确的是( )
| A. | 原子半径:Y>Z>W | |
| B. | ZW2电子式为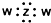 | |
| C. | 片状Y在空气中点燃时现象不剧烈 | |
| D. | 已知XW2熔点为-107℃、沸点为12.5℃,熔融时不导电,可说明固态XW2为共价化合物 |
18.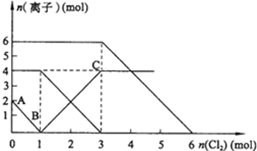 向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2═2Fe3++2Br-;2Fe3++2I-═2Fe2++I2.则下列有关说法中,不正确的是( )
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2═2Fe3++2Br-;2Fe3++2I-═2Fe2++I2.则下列有关说法中,不正确的是( )
 向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2═2Fe3++2Br-;2Fe3++2I-═2Fe2++I2.则下列有关说法中,不正确的是( )
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2═2Fe3++2Br-;2Fe3++2I-═2Fe2++I2.则下列有关说法中,不正确的是( )| A. | BC段为Fe3+的变化曲线 | |
| B. | 原混合溶液中FeBr2的物质的量为6mol | |
| C. | 当通入2mol Cl2时,溶液中发生的离子反应可表示为:2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- | |
| D. | 原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3 |
5.下列说法正确的是( )
| A. | 海水经过加碱、加酸、浓缩结晶、过滤干燥、电解制得金属镁 | |
| B. | 除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤 | |
| C. | 在稀硫酸中加入铜粉,铜粉不溶解,再加入Cu(NO3)2固体,铜粉仍不溶解 | |
| D. | 金属镁着火时,可以用二氧化碳灭火器来灭火 |
2.某炔烃与H2充分加成后的产物为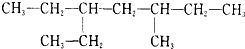 ,此炔烃可能的结构有( )
,此炔烃可能的结构有( )
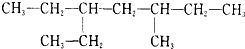 ,此炔烃可能的结构有( )
,此炔烃可能的结构有( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
3.某同学探究同周期主族元素性质递变规律时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系).
请你帮助该同学整理并完成实验报告.
(1)实验目的:探究同一周期主族元素性质的递变规律.
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液等.仪器:①烧杯,②试管,③胶头滴管,试管夹,镊子,小刀,玻璃片,砂纸,酒精灯等.
(3)实验内容:(填写与实验步骤对应的实验现象的编号和离子方程式)
(4)若用最高价氧化物的水化物的碱性相对强弱来验证Mg、Al失电子能力的相对强弱,请你设计实验(实验用品自选,不要求写化学方程式):向溶液中滴加NaOH溶液至过量,得白色沉淀,不溶解;向溶液中滴加NaOH溶液至过量,产生白色胶状沉淀,继而沉淀消失;.
(5)实验结论:同周期元素随原子序数增大,元素金属性逐渐减弱,非金属性逐渐增强.
| 实验步骤 | 实验现象 |
| 1.将镁条用砂纸打磨后,放入沸水中;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,做不定向运动,随之消失,溶液变成红色. |
| 2.向新制得的Na2S溶液中滴加少量新制的氯水 | B.有气体产生,溶液变成浅红色 |
| 3.将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体. |
| 4.将镁条投入稀盐酸中 | D.反应不十分剧烈,产生无色气体 |
| 5.将铝条投入稀盐酸中 | E.生成淡黄色沉淀 |
(1)实验目的:探究同一周期主族元素性质的递变规律.
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液等.仪器:①烧杯,②试管,③胶头滴管,试管夹,镊子,小刀,玻璃片,砂纸,酒精灯等.
(3)实验内容:(填写与实验步骤对应的实验现象的编号和离子方程式)
| 实验内容 | 实验现象 | 离子方程式 |
| 1 | ||
| 2 | ||
| 3 | ||
| 4 | ||
| 5 |
(5)实验结论:同周期元素随原子序数增大,元素金属性逐渐减弱,非金属性逐渐增强.
 .
.