题目内容
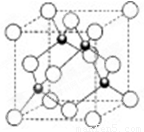
(11分)有W、X、Y、Z四种元素,其中W元素是1826年一位法国青年科学家发现的。他在研究海水制盐时,往剩余的副产物苦卤中通人氯气后,发现溶液颜色变深,再经过进一步提取可得一种红棕色有刺鼻臭味的液体,这就是W元素的单质。X、Y、Z均属短周期元素;Z元素最高正价是负价绝对值的3倍,其质子数是Y原子核内质子数的2倍,X原子核外的电子数是Z 原子的最内层上电子数的一半。
⑴W、X、Y、Z的元素符号分别是:W X Y Z
⑵W的原子结构示意图为 ,W位于第 周期 族。
⑶苦卤中通入氯气发生反应的离子方程式为 。
⑷由W元素的单质与ZY2、X2Y反应生成生成两种酸的化学方程式为 。
【答案】
⑴Br、H、O、S ⑵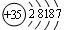 ;4;ⅦA
;4;ⅦA
⑶2Br+Cl2=Br2+2Cl- ⑷Br2+SO2+2H2O=H2SO4+2HBr
【解析】由W元素的单质呈现红棕色液体可知它必定为Br元素;
Z元素最高正价是负价绝对值的3倍,则它为第VIA族元素,可能是O或S元素;
Z原子最内层电子数为2,而X原子核外的电子数是Z 原子的最内层上电子数的一半,故X元素为H;
由(4)小题X2Y化学式可知Y元素最低负价为—2价,也为第VIA族元素;而Z原子内质子数是Y原子核内质子数的2倍,可判定Z为S元素,Y为O元素。

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
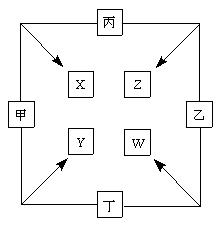
 火焰,W的水溶液呈黄色。
火焰,W的水溶液呈黄色。