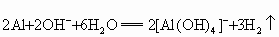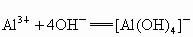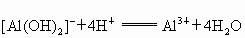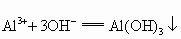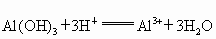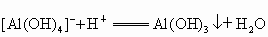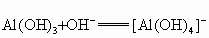题目内容
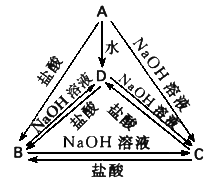
某银白色金属A,它的原子的电子层数与最外层电子数相等.在一定条件下A可以分别跟盐酸、氢氧化钠溶液和水反应,生成B、C、D,同时都有氢气生成,B.C、D在一定条件下,又可以相互转变,它们的变化如图所示,判断A,写出A、B、C、D物质间相互转化的离子方程式:A为___________;
(1)A B:_______________________________________________;
B:_______________________________________________;
(2)A C:______________________________________________;
C:______________________________________________;
(3)B C:______________________________________________;
C:______________________________________________;
(4)C B:______________________________________________;
B:______________________________________________;
(5)B D:______________________________________________;
D:______________________________________________;
(6)D B:______________________________________________;
B:______________________________________________;
(7)C D:______________________________________________;
D:______________________________________________;
(8)D C;______________________________________________.
C;______________________________________________.
答案:略
解析:
解析:
|
(1) (2) (3) (4) (5) (6) (7) (8) |

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目