题目内容
以铁为阳极,铜为阴极,对足量的NaOH溶液进行电解,一段时间后得到2 mol Fe(OH)3沉淀。此过程中共消耗水 ( )
| A.3 mol | B.4 mol | C.5 mol | D.6 mol |
C
解析

练习册系列答案
相关题目
已知电极上每通过96500C的电量就会有1mol电子发生转移.精确测量金属离子在惰性电极上以镀层形式沉积的金属质量,可以确定电解过程中通过电解池的电量.实际测量中,常用银电量计,如图所示.下列说法不正确的是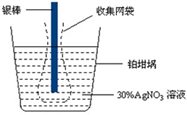
| A.电量计中的银棒应与电源的正极相连,铂坩埚上发生的电极反应是:Ag++e-=Ag |
| B.称量电解前后铂坩埚的质量变化,得金属银的沉积量为108.0mg,则电解过程中通过电解池的电量为96.5C |
| C.实验中,为了避免银溶解过程中可能产生的金属颗粒掉进铂坩埚而导致测量误差,常在银电极附近增加一个收集网袋.若没有收集网袋,测量结果会偏高 |
| D.若要测定电解饱和食盐水时通过的电量,可将该银电量计中的银棒与待测电解池的阳极相连,铂坩埚与电源的负极相连 |
Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如图所示,电解总反应为: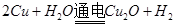 ↑。下列说法不正确的是
↑。下列说法不正确的是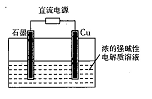
| A.石墨电极上产生氢气 |
| B.铜电极发生的电极反应为:2Cu -2e-+2OH-= Cu2O+H2O |
| C.铜电极接直流电源的正极 |
| D.当有0.1 mol电子转移时,有0.1 molCu2O生成 |
美国圣路易斯大学研制新型的乙醇燃料电池,用质子(H+)溶剂,在200oC左右供电。电池总反应为:C2H5OH+3O2→2CO2+3H2O,右图是该电池的示意图,下列说法正确的是
| A.a极为电池的正极 |
| B.电池工作时电流由a极沿导线经灯泡再到b极 |
| C.电池正极的电极反应为:4H+ + O2 + 4e-=2H2O |
| D.电池工作时,1mol乙醇被氧化时就有6mol电子转移 |
铅蓄电池是典型的可充电电池,电池总反应式为:Pb+PbO2+4H++2SO42一 2PbSO4+2H2O。下列说法正确的是
2PbSO4+2H2O。下列说法正确的是
| A.放电时,负极的电极反应式是PbO2+4H++SO42一+2e一=PbSO4+2H2O |
| B.充电时,电解液中H2SO4的浓度将变小 |
| C.放电时,PbO2发生氧化反应 |
| D.充电时,蓄电池的正极和外接电源的正极相连 |
以油类为溶剂的防锈漆称为油基防锈漆,由于环保方面的原因,目前要推广使用水基防锈漆,但水基漆较易溶解O2,在干燥之前易导致金属表面产生锈斑,为此要在水基漆中加入缓蚀剂以除去氧气,以下可作为缓蚀剂的是( )
| A.KMnO4 | B.NaNO2 | C.FeCl3 | D.HNO3 |
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,下列叙述正确的是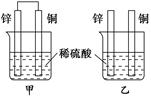
| A.两烧杯中铜片表面均无气泡产生 |
| B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的pH均增大 |
| D.产生气泡的速率甲比乙慢 |
有一新型燃料电池,是用两根金属做电极插入KOH溶液中,然后向X极通入CH4,向Y极通入O2,关于此燃料电池的说法错误的是( )
| A.通入CH4的X极是负极,通入O2的Y极是正极 |
| B.放电一段时间后,电解质溶液中KOH的物质的量不变 |
| C.在标准状况下,通入5.6 LO2,完全反应时有1.0 mol电子转移 |
| D.放电时,通入甲烷一极附近的pH升高 |
