题目内容
15.下列说法中正确的是( )| A. | 由元素的原子序数推测其在元素周期表中的位置 | |
| B. | 由H-H和Cl-Cl的键长推测液氢和液氯沸点的高低 | |
| C. | 由CaF2晶体中,与Ca2+距离最近的F-有8个,推知与F-距离最近的Ca2+也有8个 | |
| D. | 由N≡N、H-H、N-H的键能数据估算3H2(g)+N2(g)?2NH3(g)的反应热 |
分析 A、知道了元素的原子序数,可以确定元素的电子层数和最外层电子数;
B、沸点高低是物质的物理性质与共价键的键长无关;
C、萤石中每个Ca2+被8个F-所包围,每个F-周围最近距离的Ca2+数目为4;
D、在外界条件一定的情况下,反应热等于反应物的总键能-生成物的总键能.
解答 解:A、知道了元素的原子序数,可以确定元素的电子层数和最外层电子数,由电子层数确定周期数,最外层电子数确定族序数,所以由元素的原子序数推测其在元素周期表中的位置,故A正确;
B、沸点高低是物质的物理性质与共价键的键长无关,共价键的键长是决定化学性质的,故B错误;
C、萤石中每个Ca2+被8个F-所包围,每个F-周围最近距离的Ca2+数目为4,故C错误;
D、与外界条件有关,温度和压强不定,所以无法估算反应热,故D错误;
故选A.
点评 本题考查原子序数与元素在周期表中的位置、熔沸点高低的影响因素、晶体中粒子数目的比和反应热的相关知识,综合性强,但比较容易.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列各组试剂中,能用溴水加以鉴别的是( )
| A. | CH4与C3H8 | B. | 苯与己烯 | C. | 己烷与苯 | D. | 苯与甲苯 |
3.设NA代表阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 已知白磷(P4)为正四面体形,12.4 g白磷中则含有共价键数为0.4 NA | |
| B. | 3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$ Fe3O4+4H2反应中,当5.6 g Fe全部转化为Fe3O4时,则有0.3 NA电子发生转移 | |
| C. | 在0.1 mol/L碳酸钠溶液中Na+总数等于0.2 NA | |
| D. | 电解精炼铜时,当电路中转移NA个电子时,阴极增重32g |
10.下列说法不正确的是( )
| A. | 合成高效、稳定、廉价的太阳能光电转化材料,是开发利用太阳能的关键 | |
| B. | 大量焚烧田间秸秆会产生雾霾,“雾”和“霾”的分散质微粒不同 | |
| C. | 肥皂能去污的原理,是其在水溶液中能电离出钠离子(亲水基团)和硬脂酸根离子(亲油基团),在它们的共同作用下,通过搓洗,将衣服上的油污“拖下水” | |
| D. | 我国已能利用3D打印技术,以钛合金粉末为原料,通过激光熔化逐层堆积,来制造飞机钛合金结构件,高温时可用金属钠还原相应的氯化物来制取金属钛 |
20.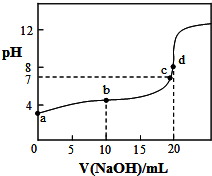 室温下,将0.1000mol/LNaOH溶液滴入20.00ml 0.1000mol/L CH3COOH溶液中,溶液pH随加入NaOH溶液体积变化曲线如图所示.下列有关说法正确的是( )
室温下,将0.1000mol/LNaOH溶液滴入20.00ml 0.1000mol/L CH3COOH溶液中,溶液pH随加入NaOH溶液体积变化曲线如图所示.下列有关说法正确的是( )
 室温下,将0.1000mol/LNaOH溶液滴入20.00ml 0.1000mol/L CH3COOH溶液中,溶液pH随加入NaOH溶液体积变化曲线如图所示.下列有关说法正确的是( )
室温下,将0.1000mol/LNaOH溶液滴入20.00ml 0.1000mol/L CH3COOH溶液中,溶液pH随加入NaOH溶液体积变化曲线如图所示.下列有关说法正确的是( )| A. | a点:由水电离出的c(H+)=1.0×10-3mol/L | |
| B. | b点:c(CH3COO-)>c(CH3COOH)>c(Na+)>c(H+)>c(OH-) | |
| C. | c点:c(Na+)=c(CH3COOH)+c(CH3COO-) | |
| D. | d点:c(OH-)-c(H+)=c(CH3COOH) |
7.铁-镍蓄电池充电放电时发生的反应为:Fe+NiO2+2H2O$?_{充电}^{放电}$Fe(OH)2+Ni(OH)2,关于此蓄电池的下列说法中不正确的是( )
| A. | 放电时负极附近溶液的碱性不变 | |
| B. | 充电时阴极的电极反应式为Ni(OH)2═NiO2+2H++2e- | |
| C. | 放电时NiO2的反应为NiO2+2e-+2H2O═Ni(OH)2+2OH- | |
| D. | 利用蓄电池电解饱和食盐水,阳极产生标准状况下8.4LCl2,则理论上电路中通过电子物质的量为0.75mol |
4.下列有关叙述中正确的是( )
| A. | 煤经过气化和液化两个物理变化,可变为清洁能源 | |
| B. | 葡萄糖可以制乙醇,两者都能与金属钠反应 | |
| C. | 明矾可用于水的消毒、杀菌;碳酸钡可用于钡餐透视 | |
| D. | 合成纤维和光导纤维都是有机高分子化合物 |
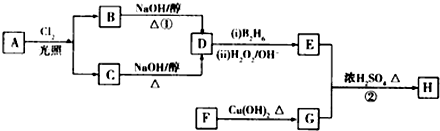
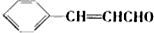 回答下列问题:
回答下列问题: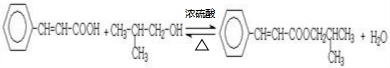 .
. .
.