题目内容
【题目】X、Y、Z、W为原子序数递增的四种短周期元素,其中Z为金属元素,X、W为同一主族元素,Y是地壳中含量最高的元素。X、Z、W分别与Y形成的最高价化合物为甲、乙、丙。结合如图转化关系,下列判断错误的是( )
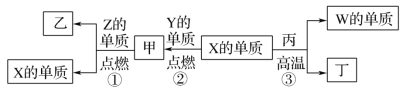
A.反应③为工业制粗硅的原理
B.Z位于元素周期表第三周期ⅡA族
C.4种元素的原子中,Y原子的半径相对最小
D.甲、丙、丁均为酸性氧化物,可以与碱反应得到对应盐
【答案】D
【解析】
由题意Y是地壳中含量最高的元素先推出Y为O元素,X、Y、Z、W为原子序数依次增大的四种短周期元素,其中Z为金属元素,可在甲中燃烧生成X的单质,应为镁与二氧化碳的反应,则Z为Mg,甲为CO2,乙为MgO,由此关系可知X为C元素,X、W为同一主族元素,则W为Si,丁为CO,丙为SiO2,以此解答该题。
由以上分析可知X为C、Y为O、Z为Mg、W为Si,甲为CO2,乙为MgO,丙为SiO2,丁为CO;
A.反应③为C与二氧化硅的反应,生成硅和CO,为工业制粗硅的原理,故A正确;
B.Z为镁,位于元素周期表第三周期ⅡA族,故B正确;
C.4种元素的原子中,Mg、Si处于第三周期,C、O处于第二周期,电子层越多,半径越大,C、O处于同周期,从左至右,半径减小,因而O的原子半径最小,故C正确;
D.甲、丙、丁分别为CO2、SiO2、CO,其中CO为不成盐氧化物,故D错误。
答案为D。

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目