题目内容
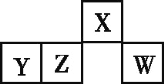
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍。下列判断正确的是
A. 原子半径:rW>rZ>rY>rX
B. 含Y元素的硫酸盐溶液可以和强酸、强 碱反应
C. 最简单气态氢化物的热稳定性: Z>W
D. X的氢化物与X的最高价氧化物对应的水化物能形成离子化合物
【答案】D
【解析】
试题W的原子的最外层电子数是最内层电子数的3倍,推出W为O或S,根据元素周期表的结构,W为S,X为N,Z为Si,Y为Al,A、半径大小比较:一看电子层数,电子层数越多,半径越大,二看原子序数,电子层数相等,半径随着原子序数的递增而减小,因此Al>Si>S>N,故错误;B、Al3+和强碱反应,不和强酸反应,故错误;C、Si的氢化物是SiH4,W的氢化物是H2S,非金属性越强,其氢化物越稳定,非金属性Si>S,故错误;D、X的氢化物是NH3,X的最高价氧化物对应的水化物是HNO3,两者发生反应生成NH4NO3,铵盐属于离子化合物,故正确。

练习册系列答案
相关题目