题目内容
9.已知下列反应:Cu+X2→CuX2、2Cu+Y→Cu2Y、2X-+Z2→2Z-+X2,X2、Y、Z2为三种元素的单质,在Cu2Y中,Y为-2价.下列关于X、Y、Z三种元素的最高价氧化物的水化物酸性由强到弱顺序正确的是( )| A. | HXO4>H2YO4>HZO4 | B. | HZO4>HXO4>H2YO4 | C. | HZO4>H2YO4>HXO4 | D. | H2YO4>HZO4>HXO4 |
分析 元素单质的氧化性越强,其元素的非金属性越强,元素的最高价氧化物的水化物的酸性越强,据此进行解答.
解答 解:根据反应Cu+X2→CuX2、2Cu+Y→Cu2Y可知,X的单质X2将铜氧化到+2价,Y能将Cu氧化到+1,所以X2的氧化性强于Y;
根据反应2KX+Z2═2KZ+X2可知:Z的氧化性强于X,所以元素的非金属性顺序是:Z>X>Y,
非金属性越强,最高价含氧酸的酸性越强,则三种元素的最高价氧化物的水化物的酸性:HZO4>HXO4>H2YO4,
故选B.
点评 本题考查学生元素的非金属性强弱的判断方法,题目难度不大,明确元素周期律的内容即可解答,注意元素的非金属性越强,元素的最高价氧化物的水化物的酸性越强.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
19.下列说法正确的是( )
| A. | 离子键就是使阴、阳离子结合成化合物的静电引力 | |
| B. | 所有金属与所有非金属原子之间都能形成离子键 | |
| C. | 因为离子键是一种强相互作用,所以离子化合物均很难分解 | |
| D. | 含有离子键的化合物一定是离子化合物 |
20.下列化学用语正确的是( )
| A. | 2-乙基-1,3-丁二烯分子的键线式: | B. | 丙烷分子的比例模型: | ||
| C. | 甲醛的电子式: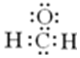 | D. | 聚丙烯的结构简式: |
17.下列关于丙烯(CH3-CH=CH2)的说法不正确的( )
| A. | 丙烯分子有8个σ键,1个π键 | |
| B. | 丙烯分子中碳原子有两种杂化方式 | |
| C. | 丙烯分子至少有六个原子在同一平面上 | |
| D. | 丙烯分子中3个碳原子在同一直线上 |
4.某有机物的分子式为C5H10O,它能发生银镜反应和加成反应,若将它与H2加成,所得产物结构简式可能是( )
| A. | (CH3)3CCH2OH | B. | (CH3CH2)2CHOH | C. | CH3(CH2)2CH(CH3)OH | D. | CH3CH2C(CH3)2OH |
18.分子式为C3H6Cl2的有机物,发生一元氯代反应后,可以生成三种同分异构体,则原C3H6Cl2的名称是( )
| A. | 1,2-二氯丙烷 | B. | 1,1-二氯丙烷 | C. | 1,3-二氯丙烷 | D. | 2,2-二氯丙烷 |

 实验室需要配制1.00mol/L NaCl溶液480mL.按下列操作步骤填上适当的文字,以使整个操作完整.
实验室需要配制1.00mol/L NaCl溶液480mL.按下列操作步骤填上适当的文字,以使整个操作完整.