题目内容
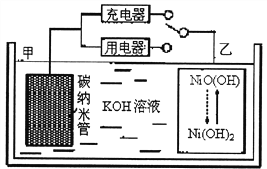
【题目】已知:pOH= -lgc(OH-)。298 K时,向20.00 mL0.10mol·L-1氨水中滴入0.10 mol·L-1的盐酸,溶液的pH和pOH与加入盐酸体积关系如图所示。下列说法正确的是
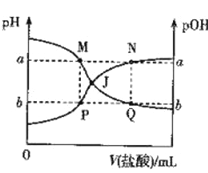
A. 曲线PJN表示溶液中PH的变化
B. M点水的电离程度比Q点大
C. M、P两点的数值之和a + b = 14
D. pH与pOH交叉点J对应的V(盐酸)=20.00 mL
【答案】C
【解析】A、此滴定实验是用盐酸滴定氨水,氨水显碱性,因此曲线PJN表示的是pOH的变化,故错误;B、曲线MJQ表示溶液中pH的变化,J点pH=pOH,此时溶液显中性,M点溶液显碱性,溶质为NH3·H2O和NH4Cl,对水的电离起抑制作用,Q点溶液显酸性,溶质可能是NH4Cl和HCl,也可能是NH4Cl,如果Q点溶质为NH4Cl,对水的电离起促进作用,因此可能Q点大于M点,故错误;C、根据图像,M点对应pH=a、pOH=b,又是常温下,因此有pH+pOH=14,故正确;D、交叉点表示溶液显中性,因为NH3·H2O是弱碱,此时的溶质为NH3·H2O和NH4Cl,消耗盐酸的体积小于20.00mL,故错误。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目