题目内容
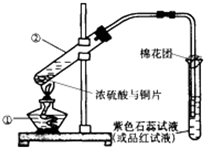
一定量的Cu粉与浓硫酸共热产生二氧化硫气体的体积为2.24L(标准状况),则下列情况不可能的是( )
| A.加入铜的质量为6.4g |
| B.加入浓硫酸中溶质0.2mol |
| C.加入铜的质量大于6.4g |
| D.加入浓硫酸中含溶质多于0.2mol |
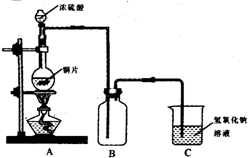
铜粉与浓硫酸混合加热,发生反应为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,n(SO2)=
=0.1mol,
A.由反应可知,n(Cu)=n(SO2)=0.1mol,则Cu的质量为0.1mol×64g/mol=6.4g,故A正确;
B.由反应可知,n(H2SO4)=0.2mol,随反应的进行,稀硫酸与Cu不反应,则加入浓硫酸中溶质应大于0.2mol,故B错误;
C.随反应的进行,稀硫酸与Cu不反应,加入Cu的质量可以大于6.4g,故C正确;
D.由B的分析可知,加入浓硫酸中含溶质多于0.2mol,故D正确;
故选:B.
| ||
| 2.24L |
| 22.4L/mol |
A.由反应可知,n(Cu)=n(SO2)=0.1mol,则Cu的质量为0.1mol×64g/mol=6.4g,故A正确;
B.由反应可知,n(H2SO4)=0.2mol,随反应的进行,稀硫酸与Cu不反应,则加入浓硫酸中溶质应大于0.2mol,故B错误;
C.随反应的进行,稀硫酸与Cu不反应,加入Cu的质量可以大于6.4g,故C正确;
D.由B的分析可知,加入浓硫酸中含溶质多于0.2mol,故D正确;
故选:B.

练习册系列答案
相关题目
 ①水解 ②加成 ③酯化 ④消去 ⑤银镜 ⑥中和。下列选项正确的( )
①水解 ②加成 ③酯化 ④消去 ⑤银镜 ⑥中和。下列选项正确的( )