题目内容
【题目】有下列4种有机化合物
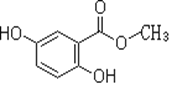
A:CH2=CH2 B:![]() C:CH3COOH D:
C:CH3COOH D: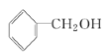
(1)写出化合物A、C中官能团的名称________、_______;
(2)4种化合物中能使溴的四氯化碳溶液褪色的是____(写名称);反应的化学方程为:_____;具有特殊气味、常做有机溶剂的是_____(写名称)。
(3)4种化合物中能与NaOH发生中和反应的是_____(写名称)。
(4)C与D在浓硫酸存在下,加热时生成的有机物的结构简式:_______。
【答案】碳碳双键 羧基 乙烯 CH2=CH2+Br2→CH2Br-CH2Br 苯 乙酸 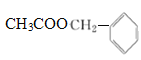
【解析】
(1)根据A、C的结构简式分析官能团;
(2)烯烃能与溴的四氯化碳溶液发生加成反应;苯是常见的有机溶剂;
(3)羧酸能与NaOH发生中和反应;
(4)羧酸与醇在浓硫酸存在下发生酯化反应生成酯和水;
(1)A是乙烯,官能团是碳碳双键,C是乙酸,官能团是羧基;
(2)乙烯含有碳碳双键可与溴水发生加成反应是溴水褪色,反应的化学方程式为:CH2=CH2+Br2→CH2Br-CH2Br;苯是有特殊香味的液体,是常见的有机溶剂;
(3)能与NaOH发生中和反应则该物质具有酸性,三种物质中有酸性的是乙酸;
(4)CH3COOH与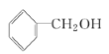 在浓硫酸存在下发生酯化反应,生成的酯的结构简式是
在浓硫酸存在下发生酯化反应,生成的酯的结构简式是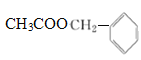 。
。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】煤燃烧排放的烟气含有SO2和NOx,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,回答下列问题:
(1) NaClO2的化学名称为_______。
(2)在鼓泡反应器中通入含有含有SO2和NOx的烟气,反应温度为323 K,NaClO2溶液浓度为5×103mol·L1。反应一段时间后溶液中离子浓度的分析结果如下表》
离子 | SO42 | SO32 | NO3 | NO2 | Cl |
c/(mol·L1) | 8.35×104 | 6.87×106 | 1.5×104 | 1.2×105 | 3.4×103 |
①写出NaClO2溶液脱硝过程中主要反应的离子方程式__________。增加压强,NO的转化率______(填“提高”“不变”或“降低”)。
②随着吸收反应的进行,吸收剂溶液的pH逐渐______ (填“提高”“不变”或“降低”)。
③由实验结果可知,脱硫反应速率______脱硝反应速率(填“大于”或“小于”)。原因是除了SO2和NO在烟气中的初始浓度不同,还可能是___________。
(3)在不同温度下,NaClO2溶液脱硫、脱硝的反应中,SO2和NO的平衡分压px如图所示。
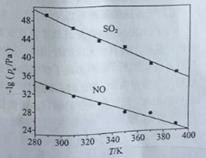
①由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均______________(填“增大”“不变”或“减小”)。
②反应ClO2+2SO32===2SO42+Cl的平衡常数K表达式为___________。
(4)如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果。
①从化学平衡原理分析,Ca(ClO)2相比NaClO具有的有点是_______。
②已知下列反应:
SO2(g)+2OH(aq) ===SO32(aq)+H2O(l) ΔH1
ClO(aq)+SO32(aq) ===SO42(aq)+Cl(aq) ΔH2
CaSO4(s) ===Ca2+(aq)+SO42(aq) ΔH3
则反应SO2(g)+ Ca2+(aq)+ ClO(aq) +2OH(aq) ="==" CaSO4(s) +H2O(l) +Cl(aq)的ΔH=______。