题目内容
【题目】钛镍合金被称为记忆合金,是一种具有独特形状记忆功能、耐磨损、抗腐蚀、超弹性等特点的功能材料,主用于航空航天、医疗等领域。回答下列问题:
(1)基态镍原子的价电子排布式为 __________,其所在周期第一电离能最小的元素名称为__。
(2)钛铁矿经过 H2SO4、HNO3等多种物质处理后会生成硫酸氧钛等中间产物。
①硫酸氧钛晶体中阳离子为如图1所示链状聚合形式的离子,该晶体的化学式为_,晶体中存在的微粒间作用力有离子键、___和____。

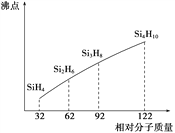
②查资料知H2SO4和HNO3的沸点分别为338℃和83℃,试分析差异大的主要原因__。
(3)镍是人体必需的微量元素,但超量中毒易过敏或诱发癌症。急性镍中毒通常用二乙基二硫代氨基钠(结构如图2)解毒,该物质中碳原子的杂化方式有___。

(4)Ni、O、Cr 可以形成一种具有特殊导电性的复合氧化物晶胞结构如图3。若晶胞参数为apm,晶胞中Cr4+位于O2-所形成的正八面体的体心,该正八面体的边长为__pm。设阿伏加德罗常数数值为NA,则该晶体密度为__g·cm-3。

【答案】![]() 钾 TiOSO4 共价键 配位键 H2SO4只能形成分子间氢键,HNO3能形成分子内氢键 sp2、sp3
钾 TiOSO4 共价键 配位键 H2SO4只能形成分子间氢键,HNO3能形成分子内氢键 sp2、sp3 ![]() a
a 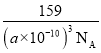
【解析】
(1)镍为28号元素,基态镍原子的价电子排布式为![]() ,同周期元素第一电离能有依次增大的趋势。镍为第四周期,所在周期第一电离能最小的元素名称为钾。
,同周期元素第一电离能有依次增大的趋势。镍为第四周期,所在周期第一电离能最小的元素名称为钾。
(2)①如图在阳离子中每个O原子被两个Ti原子共用、每个Ti原子被两个O原子共用,利用均摊法可知,每个钛原子实际占有的氧原子为2×![]() =1,所以二者原子个数之比为1:1。所以晶体的化学式为TiOSO4,S和OTi中的O形成一般的共价键,然后S还有4个电子,分别和两个O形成配位键,分子中存在离子键、共价键和配位键。
=1,所以二者原子个数之比为1:1。所以晶体的化学式为TiOSO4,S和OTi中的O形成一般的共价键,然后S还有4个电子,分别和两个O形成配位键,分子中存在离子键、共价键和配位键。
②H2SO4和HNO3除了含有共价键之外,都能够形成氢键,H2SO4只能形成分子间氢键,HNO3能形成分子内氢键。
(3)根据结构图2,分子中有碳双键,该碳为sp2杂化,分子中有甲基,碳原子为sp3杂化。
(4)正八面体的两个顶点与体心原子形成等腰直角三角形,正八面体的边长等于该等腰直角三角形的直角边长度的![]() 倍,而等腰直角三角形的直角边长度等于晶胞棱长的一半,故该正八面体的边长为:
倍,而等腰直角三角形的直角边长度等于晶胞棱长的一半,故该正八面体的边长为:![]() a pm;晶胞质量=
a pm;晶胞质量=![]() g,晶体密度=
g,晶体密度=![]() g÷(a×10-10cm)3
g÷(a×10-10cm)3
即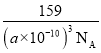

【题目】POC13常用作半导体掺杂剂及光导纤维原料,实验室制备POC13并测定产品含量的实验过程如下:
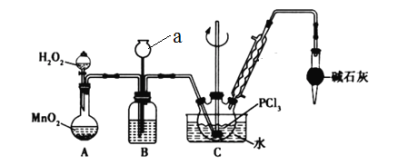
I.实验室制备POC13。采用氧气氧化液态PCl3法制取POC13,实验装置(加热及夹持仪器略)如下图:
资料:①Ag++SCN-=AgSCN↓ Ksp(AgCl)>Ksp(AgSCN);
②PCl3和POC13的相关信息如下表:
物质 | 熔点/℃ | 沸点/℃ | 相对分子质量 | 其他 |
PCl3 | -112.0 | 76.0 | 137.5 | 两者互溶,均为无色液体,遇水均剧烈反应生成含氧酸和氯化氢 |
POC13 | 2.0 | 106.0 | 153.5 |
(1)仪器a的名称____________________。
(2)B中所盛的试剂是________,干燥管的作用是_____________________。
(3)POC13遇水反应的化学方程式为____________________________。
(4)反应温度要控制在60~65℃,原因是:____________________________。
II.测定POC13产品的含量。实验步骤:
①制备POC13实验结束后,待三颈瓶中的液体冷却至室温,准确称取29.1g产品,置于盛有60.00 mL蒸馏水的水解瓶中摇动至完全水解,将水解液配成100.00 mL溶液。
②取10.00 mL溶液于锥形瓶中,加入20.00 mL 3.5mol/L AgNO3标准溶液。
③加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖。
④以X为指示剂,用1.00mol/LKSCN溶液滴定过量AgNO3溶液,达到滴定终点时共用去10.00mLKSCN溶液。
(5)步骤④中X可以选择___________________ 。
(6)步骤③若不加入硝基苯,会导致测量结果______(填偏高,偏低,或无影响)
(7)反应产物中POC13的质量百分含量为___________________, 若滴定终点,读取KSCN溶液俯视刻度线,则上述结果____________(填偏高,偏低,或无影响)