题目内容
已知某溶液中只存在OH-、H+、CH3COO-、Na+四种离子,且其离子浓度的大小顺序为:c(Na+)>c(OH-)>c(CH3COO-)>c(H+),则原溶液中溶质为A.CH3COONa B.CH3COONa、NaOH
C.CH3COOH、CH3COONa D.CH3COOH、NaCl
解析:该题主要考查离子浓度大小关系和溶液中溶质的成分分析。A选项,CH3COONa在水溶液中发生水解使溶液呈碱性,但水解程度较弱,所以c(CH3COO-)虽然略小于c(Na+)但远大于c(OH-),故不正确。B选项,由于存在NaOH,抑制了c(CH3COO-)水解,且NaOH所占比例较多,c(OH-)>c(CH3COO-),所以正确。C选项,由于存在CH3COOH和c(CH3COO-),二者相互抑制了水解和电离,所以不可能存在c(OH-)>c(CH3COO-)的关系,所以不正确。D项,溶液呈酸性,c(H+)>c(OH-),故不正确。
答案:B

练习册系列答案
相关题目
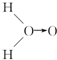 (式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)
(式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)
 的沸点高于
的沸点高于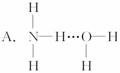

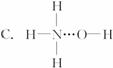

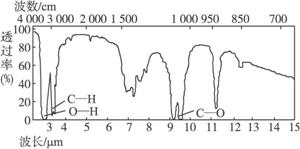
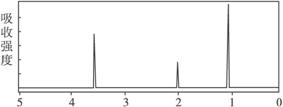
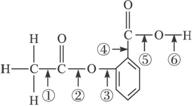
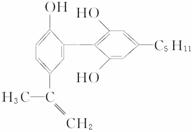


 子反应式: 。
子反应式: 。