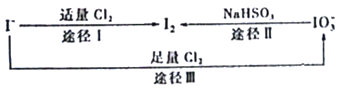
题目内容
【题目】二氧化铈(CeO2)是一种重要的稀土氧化物,平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2、FeO等物质)。某课题组以此粉末为原料,设计如下工艺流程对资源进行回收,得到纯净的CeO2和硫酸铁铵晶体。
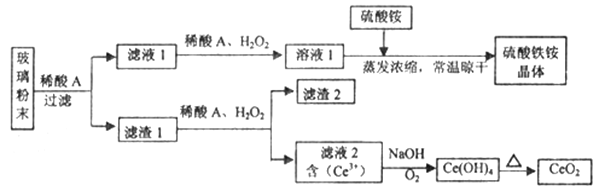
已知:CeO2不溶于稀硫酸,也不溶于NaOH溶液。
回答下列问题:
(1)滤液1中加入H2O2溶液的目的是____________________________________________________。
(2)设计实验证明滤液1中含有Fe2+__________________________________________________________。
(3)在酸性溶液中,已知Fe2+溶液可以和难溶于水的FeO(OH)反应生成Fe3O4,书写该反应的离子方程式____________________________________________________________________。
(4)由滤液2生成Ce(OH)4的离子方程式______________________________________________。
(5)取上述流程中得到的Ce(OH)4产品0.531 g,加硫酸溶解后,用浓度为0.l000 mol·L-1的FeSO4标准溶液滴定至终点时(铈被还原为Ce3+ ),消耗25.00 mL标准溶液。该产品中Ce(OH)4的质量分数为______________ (结果保留两位有效数字),Mr(Ce)=140。
【答案】使Fe2+氧化为Fe3+ 取少许滤液1,滴加铁氰化钾溶液,有蓝色沉淀生成,则证明滤液1中有Fe2+ Fe2+ +2FeO(OH) == Fe3O4 +2H+ 4Ce3 ++ O2 +12OH-+2H2O ==4Ce(OH)4↓ 0.98或98%
【解析】
反应过程为:废玻璃粉末(含SiO2、Fe2O3、CeO2、FeO等物质)中加入稀硫酸,FeO转化为FeSO4、Fe2O3转化Fe2(SO4)3存在于滤液1中,滤渣1为CeO2和SiO2;
滤液1中加入稀硫酸和H2O2,使FeSO4氧化为Fe2(SO4)3,溶液1为Fe2(SO4)3溶液,加入硫酸铵混合蒸发浓缩、常温晾干后得到硫酸铁铵晶体;
滤渣1中加入稀硫酸和H2O2,CeO2转化为Ce3+存在于滤液2中,反应为2CeO2+H2O2+3H2SO4=Ce2(SO4)3+O2↑+4H2O,滤渣2为SiO2;滤液2加入碱并通入氧气将Ce从+3氧化为+4后Ce3+转化为沉淀Ce(OH)4,反应为:4Ce3++O2+12OH-+2H2O═4Ce(OH)4↓,加入分解Ce(OH)4得到产品CeO2;据此分析作答。
(1)已知:CeO2不溶于稀硫酸,废玻璃粉末(含SiO2、Fe2O3、CeO2、FeO等物质)中也不SiO2溶于酸,加入稀硫酸可将CeO2和SiO2与Fe2O3、FeO分离,滤液1中加入H2O2的目的是使Fe2+氧化为Fe3+;
(2)亚铁离子有还原性能使酸性高锰酸钾褪色,也与铁氰化钾生成蓝色沉淀,故证明滤液1中含有Fe2+方法为:取少许滤液1,滴加铁氰化钾溶液,有蓝色沉淀生成,则证明滤液1中有Fe2+;
(3)已知Fe2+溶液可以和难溶于水的FeO(OH)反应生成Fe3O4,根据电子得失守恒和原子守恒可知该反应的离子方程式为Fe2+ +2FeO(OH) == Fe3O4 +2H+;
(4)滤液2为含有Ce3+的溶液,加入碱并通入氧气将Ce从+3氧化为+4后Ce3+转化为沉淀Ce(OH)4,离子方程式为:4Ce3 ++ O2 +12OH-+2H2O ==4Ce(OH)4↓;
(5)用0.1000mol/LFeSO4溶液滴定至终点,铈被还原成Ce3+,则Fe2+被氧化为Fe3+,则 Ce(OH)4~Ce3+~FeSO4, 所以n[Ce(OH)4]=n(FeSO4)=0.1×25×10-3mol,m[Ce(OH)4]=0.1×25×10-3×208g,该产品中Ce(OH)4的纯度的表达式为![]() ×100=98%。
×100=98%。