题目内容
【题目】(1)碱洗铝材除其表面的氧化膜,碱洗时常有气泡冒出,原因是___(用离子方程式表示)。为将碱洗后溶液中的铝以沉淀形式回收,最好应加入下列试剂中的____(填字母)。
a.稀H2SO4 b.盐酸 c.CO2 d.氨水 e.NaOH
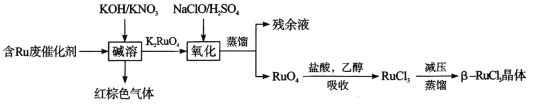
(2)某校化学兴趣小组用如图所示过程除去AlCl3中含有的Mg2+、K+杂质离子并尽可能减少AlCl3的损失。请回答下列问题:
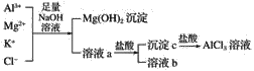
①写出混合物中加入足量氢氧化钠溶液时,溶液中发生反应的离子方程式:___,__,___。
②氢氧化钠溶液能否用氨水代替,为什么?___。
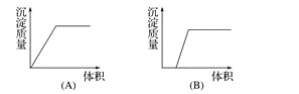
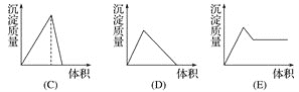
③溶液a中存在的离子有___,在溶液a中加入盐酸时需控制盐酸的量,为什么?___,为此,改进方法是___。
【答案】2Al+2OH-+2H2O=2AlO2-+3H2↑ c Mg2++2OH-=Mg(OH)2↓ Al3++3OH-=Al(OH)3↓ Al(OH)3+OH-=AlO2-+2H2O(或者写Al3++4OH-=AlO2-+2H2O) 不能,因为在Al3+与氨水反应生成Al(OH)3后,Al(OH)3不能与氨水继续反应,从而不能将Al(OH)3与Mg(OH)2分开 Cl-、K+、AlO2-、OH-、Na+ 因为氢氧化铝能与强酸反应,所以在加入盐酸沉淀AlO2-时,需要控制盐酸的量,以防止部分AlO2-转化成Al3+ 通入过量二氧化碳气体
【解析】
(1)铝材表面的Al2O3与碱反应后,Al会与碱反应生成氢气;
(2)Al3+、Mg2+会与OH-反应生成沉淀,但是Al(OH)3会溶于过量的碱,转化为AlO2-,AlO2-与酸反应生成Al(OH)3。
(1)冒气泡的原因是表面Al2O3与碱液反应后Al与强碱溶液反应生成H2,碱洗液中Al元素以AlO2-形式存在,为防止Al(OH)3溶解,应通入CO2使AlO2-转化为Al(OH)3,答案是2Al+2OH-+2H2O=2AlO2-+3H2↑ c;
(2)①加入足量氢氧化钠溶液,Mg2+可与OH-反应生成Mg(OH)2沉淀,Al3+先与OH-反应生成Al(OH)3,生成的Al(OH)3继续与OH-反应生成NaAlO2和H2O;答案为Mg2++2OH-=Mg(OH)2↓; Al3++3OH-=Al(OH)3↓ ;Al(OH)3+OH-=AlO2-+2H2O(或者写Al3++4OH-=AlO2-+2H2O);
②氢氧化钠溶液不能用氨水代替,因为在Al3+与氨水反应生成Al(OH)3后,Al(OH)3不能与氨水继续反应,从而不能将Al(OH)3与Mg(OH)2分开;
③加入氢氧化钠溶液后除去了Mg2+,但又引入了Na+,同时Al3+转化成了AlO2-;因为氢氧化铝能与强酸反应,所以在加入盐酸沉淀AlO2-时,需要控制溶液的pH,以防止部分AlO2-转化成Al3+;氢氧化铝只能与强碱或强酸反应,因此,可在溶液a中通入过量二氧化碳气体。

 走进文言文系列答案
走进文言文系列答案