题目内容
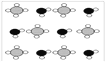
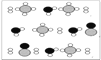
【题目】根据下图所示实验,判断下列叙述错误的是

A. 如图所示实验能够证明碳酸的酸性强于硅酸
B. 如图所示实验可证明元素的非金属性:Cl>C>Si
C. 如图所示实验中没有可以设计原电池的化学反应
D. 如图实验开始前需要打开分液漏斗的上口瓶塞
【答案】B
【解析】
A.利用饱和碳酸氢钠溶液除去二氧化碳中的氯化氢,然后通入硅酸钠溶液中产生硅酸,因此该实验能够证明碳酸的酸性强于硅酸,A正确;B. 盐酸不是氯元素的最高价含氧酸,是无氧酸,不能证明元素的非金属性:Cl>C>Si,B错误;C. 如图所示实验中均是复分解反应,不是氧化还原反应,因此没有可以设计原电池的化学反应,C正确;D. 为了使分液漏斗中的液体顺利流下,实验开始前需要打开分液漏斗的上口瓶塞,使内外压强相等,D正确,答案选B。

练习册系列答案
相关题目