题目内容
【题目】在25℃时向VmL pH=m的HNO3中,滴加pH=n的KOH溶液10 V mL时,溶液中NO3-物质的量恰好等于加入的K+的物质的量,则m+n的值为 ( )
A. 13 B. 14 C. 15 D. 不能确定
【答案】A
【解析】试题分析:根据题意知溶液中NO3﹣的物质的量恰好等于加入K+的物质的量,则HNO3和KOH恰好完全反应,溶液呈中性,则n(HNO3)=n(KOH)。VmLpH=m的HNO3溶液中n(HNO3)=V×10-3L×10-mmol/L,10VmL pH=n的KOH溶液中n(KOH)=10V×10-3L×10n-14mol/L,解得:m+n=13,选A。

练习册系列答案
相关题目
【题目】高纯六水氯化锶晶体(SrCl26H2O)具有很高的经济价值,工业上用难溶于水的碳酸锶(SrCO3)为原料(含少量钡和铁的化合物等),制备高纯六水氯化锶晶体的过程为: 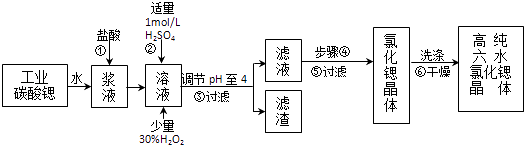
已知:Ⅰ.SrCl26H2O晶体在61℃时开始失去结晶水,100℃时失去全部结晶水.
Ⅱ.有关氢氧化物开始沉淀和完全沉淀的pH表:
氢氧化物 | Fe(OH)3 | Fe(OH)2 |
开始沉淀的pH | 1.5 | 6.5 |
沉淀完全的pH | 3.7 | 9.7 |
(1)操作①加快反应速率的措施有(写一种).碳酸锶与盐酸反应的离子方程式 .
(2)酸性条件下,加入30% H2O2溶液,将Fe2+氧化成Fe3+ , 其离子方程式为 .
(3)在步骤②﹣③的过程中,将溶液的pH值由1调节至4时,宜用的试剂为
A.氨水
B.氢氧化锶粉末
C.氢氧化钠
D.碳酸钠晶体
(4)操作③中所得滤渣的主要成分是(填化学式).
(5)步骤④的操作是、 .
(6)工业上用热风吹干六水氯化锶,适宜的温度是
A.50~60℃
B.70~80℃
C.80~100℃
D.100℃以上.

