题目内容
短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的气态化合物的水溶液呈碱性,乙位于第VA族,甲和丙同主族,丁的最外层电子数和电子层数相等,则
| A.原子半径:丙<丁<乙 | B.乙、丙、丁的最高价氧化物对应的水化物能相互反应 |
| C.甲、乙、丙的氧化物均为共价化合物 | D.单质的还原性:丁>丙>甲 |
B
解析试题分析:气态化合物的水溶液呈碱性为氨气,故甲、乙、丙、丁分别为H、N、Na、Al。A、原子半径
乙<丁<丙,错误;B、乙、丙、丁的最高价氧化物对应的水化物分别为强酸、强碱、两性氢氧化物,故能相互反应,正确;C、氧化钠为离子化合物,错误;D、单质还原性丙>丁>甲,错误。
考点:考查元素周期律与周期表的有关问题。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
随着卤素原子半径的增大,下列递变规律正确的是
| A.单质熔、沸点逐渐降低 | B.气态氢化物稳定性逐渐增强 |
| C.卤素离子的还原性逐渐增强 | D.元素的非金属性逐渐增强 |
下列有关原子结构或元素性质说法正确的是
| A.原子核外电子排布式为1s2的元素与原子核外电子排布式为1s22s2的元素化学性质相似 |
B.基态碳原子的价电子排布图: |
C.基态铜原子的价电子排布图: |
| D.Fe3+的最外层电子排布式为:3s23p63d5 |
X、Y、Z、W四种短周期元素在周期表的位置如图,Y原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是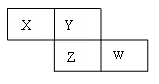
| A.气态氢化物的稳定性:X>Y |
| B.Z元素的氧化物对应的水化物一定是一种强酸 |
| C.X、Y、Z原子半径的大小顺序: X>Y>Z |
| D.X的气态氢化物与W的气态氢化物可以相互反应 |
下列说法正确的是
| A.第ⅦA族元素的非金属性比第ⅥA族元素的强 |
| B.第三周期元素的简单阳离子半径从左到右逐渐减小 |
| C.第ⅤA族元素非金属氧化物对应的水化物的酸性从上到下依次减弱 |
| D.依据元素周期表、周期律推测尚未发现的第七周期第ⅦA族元素应为非金属元素 |
2012年,IUPAC正式命名了116号元素,但117号元素尚未被正式认定。下列关于 的说法,错误的是
的说法,错误的是
| A.是两种原子 | B.互为同位素 |
| C.中子数分别为176和177 | D.电子数相差1 |
