题目内容
【题目】下列实验能成功的是
A. 用 1体积的乙醇与3体积的浓H2SO4混合加热到140℃制乙烯
B. 加入适量浓溴水除去苯中混有的少量苯酚
C. 用饱和食盐水和电石(CaC2)制乙炔
D. 以盐酸、石灰石、苯酚钠溶液为试剂,验证酸性强弱关系:盐酸>石炭酸>碳酸
【答案】C
【解析】
试题分析:A.用1体积的乙醇与3体积的浓H2SO4混合加热到170℃制乙烯,A项错误;B.苯酚与溴水反应生成的三溴苯酚易溶于苯,引入新杂质,B项错误;C.电石与水反应生成乙炔,但该反应非常剧烈,为了减慢反应速率,用饱和食盐水和电石反应制取乙炔,C项正确;D.根据强酸可以制取弱酸来判断,酸性:盐酸>碳酸>石炭酸,D项错误;答案选C。

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
【题目】(1)容量瓶上含有下列量中的(填写字母) 。
A压强 B温度 C容积 D密度 E刻度线
(2)用浓硫酸配制250mL2molL-1硫酸溶液时,所需的玻璃仪器除烧杯、玻璃棒和胶头滴管之外,还需要 (填仪器名称);在下列配制过程示意图中,有错误的是(填写序号) 。
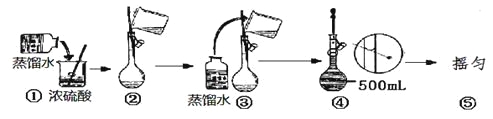
(3)下列情况将使配制溶液的物质的量浓度偏低的有 (填序号)
A.容量瓶用蒸馏水洗净后未待干燥便用来配制 |
B.NaOH溶解后趁热移入容量瓶中 |
C.定容时,俯视刻度线 |
D.摇匀后发现液面未到刻度线,继续加水至刻度线 |