题目内容
【题目】AF是几种烃分子的球棍模型(如下图所示),据此冋答下列问题:
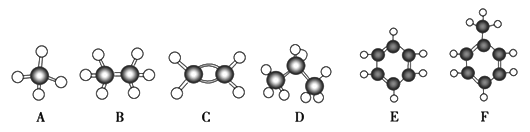
(1)含碳量最高的烃是(填对应字母)____________________
(2)能够发生加成反应的烃有(填对应字母)__________________
(3)写出F与液溴反应的化学方程式__________________
【答案】 F C、E、F ![]()
【解析】本题分析:本题主要考查烃的性质。A、B、C、D、E、F分别是甲烷、乙烷、乙烯、丙烷、甲苯、苯,它们的分子组成分别是CH4、C2H6、C2H4、C3H8、C7H8、C6H6。
(1)烃的分子组成CxHy可表示为(![]() )x,含碳量最高的是
)x,含碳量最高的是![]() 最小的烃,故选F。
最小的烃,故选F。
(2)能够发生加成反应的烃是具有不饱和结构的C、E、F。
(3)F与液溴反应的化学方程式为![]() 。
。

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目