题目内容
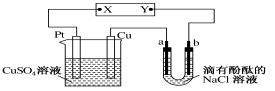
【题目】由U形管、铁棒、石墨棒、1 L 0.lmol/L CuCl2溶液等组成如图装置,下列说法不正确的是
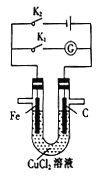
A. 同时打开K1、K2,铁棒上有紫红色物质析出
B. 只闭合K1,石墨棒上有紫红色物质析出
C. 只闭合K2,当电路中通过0.3mol电子时,两极共产生4.48L(标准状况)气体
D. 只闭合K2,一段时间后,将电解质溶液搅拌均匀,溶液的pH变大(不考虑Cl2的溶解)
【答案】C
【解析】A、同时打开K1和K2,此装置不是闭合回路,铁把铜置换出来,发生Fe+Cu2+=Fe2++Cu,铜单质附着在铁表面,故A说法正确;B、只闭合K1,构成原电池,铁作负极,石墨作正极,正极上电极反应式为Cu2++2e-=Cu,故B说法正确;C、只闭合K2,构成电解池,铁作阴极,石墨作阳极因为1L0.1mol·L-1的CuCl2溶液,n(Cl-)=0.2mol,n(Cu2+)=0.1mol,当电路中通过0.3mol电子时,阳极电极反应式为2Cl-2e-=Cl2↑,阴极电极反应式为Cu2++2e-=Cu
0.2 0.2 0.1 0.1 0.2 0.2 通过0.3mol电子,因此还要电解水,阳极电极反应式为4OH--4e-=O2↑+H2O,
0.1 0.1/4 阴极电极反应式为2H++2e-=H2↑
0.1 0.1/2,因此两极上收集到气体的物质的量为(0.1+0.1/4+0.1/2)mol=0.175mol,因此标准状况下,气体体积为0.175×22.4L=3.92L,故C说法错误;D、只闭合K2,构成电解池,CuCl2溶液中Cu2+水解,Cu2++2H2O ![]() Cu(OH)2+2H+,使CuCl2溶液显酸性,电解过程中消耗Cu2+,因此电解一段时间后溶液的pH增大,故D说法正确。
Cu(OH)2+2H+,使CuCl2溶液显酸性,电解过程中消耗Cu2+,因此电解一段时间后溶液的pH增大,故D说法正确。

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目